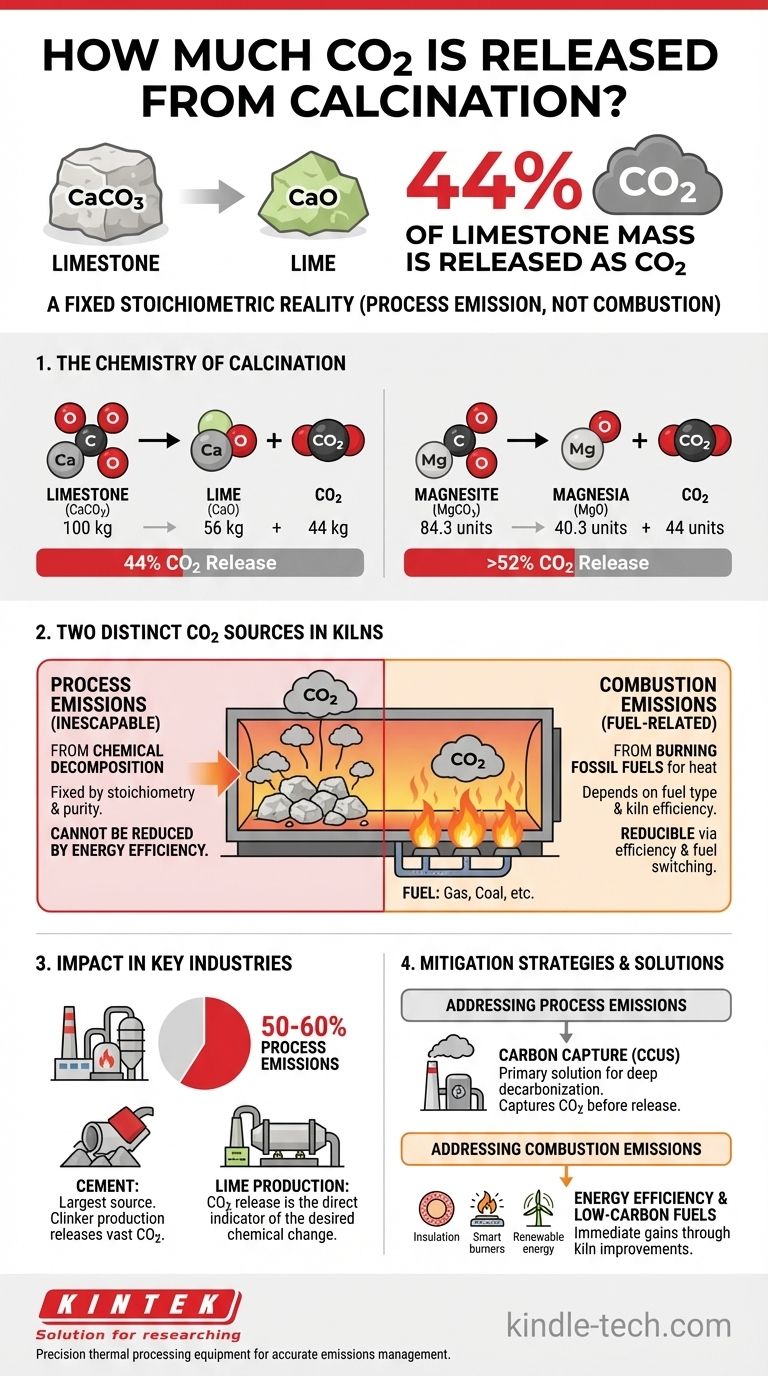
A calcinação do calcário (carbonato de cálcio) libera 44% de sua massa como dióxido de carbono. Para cada 1.000 kg de carbonato de cálcio puro que é processado, 440 kg de CO2 são inevitavelmente liberados como resultado direto da transformação química.
O princípio fundamental a ser compreendido é que o CO2 liberado durante a calcinação é uma emissão de processo, não uma emissão de combustão. Ele é liberado diretamente da estrutura química da matéria-prima, tornando-o uma parte inescapável da reação, independente do combustível utilizado para aquecimento.

A Química da Calcinação: Uma Realidade Estequiométrica
A calcinação é um processo de decomposição térmica. Quando certos materiais, particularmente carbonatos, são aquecidos a uma alta temperatura, eles se decompõem em um novo sólido (geralmente um óxido) e liberam um gás.
Carbonato de Cálcio (Calcário)
O exemplo industrial mais comum é a calcinação do calcário (CaCO3) para produzir cal (CaO).
A equação química balanceada é: CaCO3 → CaO + CO2
Ao observar as massas atômicas (Ca≈40, C≈12, O≈16), podemos ver que 100 unidades de CaCO3 se decompõem em 56 unidades de CaO e 44 unidades de CO2. Esta relação de massa de 44% é um fato químico fixo.
Carbonato de Magnésio (Magnesita)
Uma reação semelhante ocorre para o carbonato de magnésio (MgCO3), que é calcinado para produzir magnésia (MgO).
A equação é: MgCO3 → MgO + CO2
Aqui, aproximadamente 84,3 unidades de MgCO3 se decompõem em 40,3 unidades de MgO e 44 unidades de CO2. Isso significa que para a magnesita, mais de 52% da massa inicial é liberada como CO2.
A Fonte do Dióxido de Carbono
É fundamental reconhecer que este CO2 estava quimicamente preso na própria rocha. O calor elevado simplesmente fornece a energia necessária para quebrar as ligações químicas e liberar o gás que já estava presente na estrutura molecular do material.
Emissões de Processo vs. Emissões de Combustão
Em qualquer forno do mundo real, existem duas fontes distintas de CO2, e a falha em diferenciá-las leva a uma confusão significativa na gestão de emissões.
Emissões de Processo (O CO2 Inescapável)
Este é o CO2 liberado da decomposição química da matéria-prima carbonática, conforme descrito acima. É determinado inteiramente pela estequiometria da reação e pela pureza da matéria-prima.
Emissões de Combustão (O CO2 Relacionado ao Combustível)
Este é o CO2 gerado pela queima de combustíveis fósseis (como gás natural, carvão ou coque de petróleo) para atingir as altas temperaturas (frequentemente >900°C) necessárias para a calcinação. Esta porção das emissões depende do tipo de combustível e da eficiência térmica do forno.
Por Que Essa Distinção É Crucial
Você pode reduzir as emissões de combustão melhorando o isolamento do forno, usando queimadores mais eficientes ou mudando para combustíveis de baixo carbono. No entanto, você não pode reduzir as emissões de processo através da eficiência energética. O CO2 da rocha será liberado independentemente de você aquecê-la com gás natural, eletricidade ou energia solar concentrada.
O Impacto da Calcinação nas Principais Indústrias
A liberação estequiométrica de CO2 torna a calcinação um foco principal para os esforços de descarbonização industrial.
A Indústria Cimenteira
A fabricação de cimento é a maior fonte única de emissões de calcinação globalmente. A produção de clínquer, o ingrediente chave do cimento, envolve a calcinação de enormes quantidades de calcário.
As emissões de processo da calcinação representam 50-60% da pegada total de CO2 das modernas fábricas de cimento. O restante provém da combustão de combustível.
Produção de Cal
O propósito de um forno de cal é produzir CaO a partir de CaCO3. Portanto, a liberação de CO2 não é apenas um subproduto, mas um indicador direto de que a transformação química desejada ocorreu.
Armadilhas Comuns e Estratégias de Mitigação
Compreender a natureza das emissões de calcinação é fundamental para desenvolver estratégias eficazes para gerenciá-las.
A Armadilha da Ineficiência
Um erro comum é acreditar que tornar um forno mais eficiente energeticamente eliminará suas emissões de CO2. Embora este seja um passo crítico para reduzir as emissões de combustão, não faz absolutamente nada para interromper as emissões de processo.
O Papel da Captura de Carbono
Como as emissões de processo são quimicamente inevitáveis, a principal solução tecnológica para a descarbonização profunda em setores como cimento e cal é a Captura, Utilização e Armazenamento de Carbono (CCUS). Esta tecnologia captura o CO2 dos gases de combustão antes que ele entre na atmosfera.
Materiais Alternativos
A pesquisa de longo prazo se concentra no desenvolvimento de materiais de construção alternativos que não dependam da calcinação de carbonatos, eliminando assim o problema do processo por completo.
Como Quantificar o CO2 para Seu Processo
Sua abordagem para medir e gerenciar o CO2 dependerá de seu objetivo específico. Use os princípios da estequiometria como sua base.
- Se seu foco principal é a relatoria precisa de emissões: Você deve calcular as emissões de processo com base na massa e composição química de sua matéria-prima carbonática, e então calcular separadamente as emissões de combustão com base nos dados de consumo de combustível.
- Se seu foco principal é a redução de emissões: Direcione as emissões de combustão primeiro através da eficiência energética e da troca de combustível para ganhos imediatos, enquanto avalia a captura de carbono como a solução de longo prazo para as emissões de processo inevitáveis.
- Se seu foco principal é o projeto de processo e o balanço de massa: Considere a perda significativa de massa (44% para calcário puro) de sua matéria-prima sólida à medida que ela se converte em gás, pois isso impactará fundamentalmente os fluxos de material e os cálculos de rendimento do produto.
Compreender a natureza fixa e estequiométrica das emissões de calcinação é o primeiro e mais crítico passo para gerenciar a pegada de carbono desses processos industriais essenciais.
Tabela Resumo:
| Material | Reação Química | Aprox. CO2 Liberado (em massa) |
|---|---|---|
| Calcário (CaCO3) | CaCO3 → CaO + CO2 | 44% |
| Magnesita (MgCO3) | MgCO3 → MgO + CO2 | >52% |
Precisa de equipamento de processamento térmico preciso para gerenciar seu processo de calcinação e suas emissões? A KINTEK é especializada em fornos e estufas de laboratório de alto desempenho projetados para controle preciso de temperatura e eficiência de processo. Seja em P&D, produção de cimento ou cal, nossos equipamentos ajudam você a alcançar resultados ótimos, fornecendo os dados necessários para uma contabilidade precisa de emissões. Entre em contato com nossos especialistas hoje para discutir como nossas soluções podem apoiar seus objetivos específicos de calcinação e descarbonização.
Guia Visual