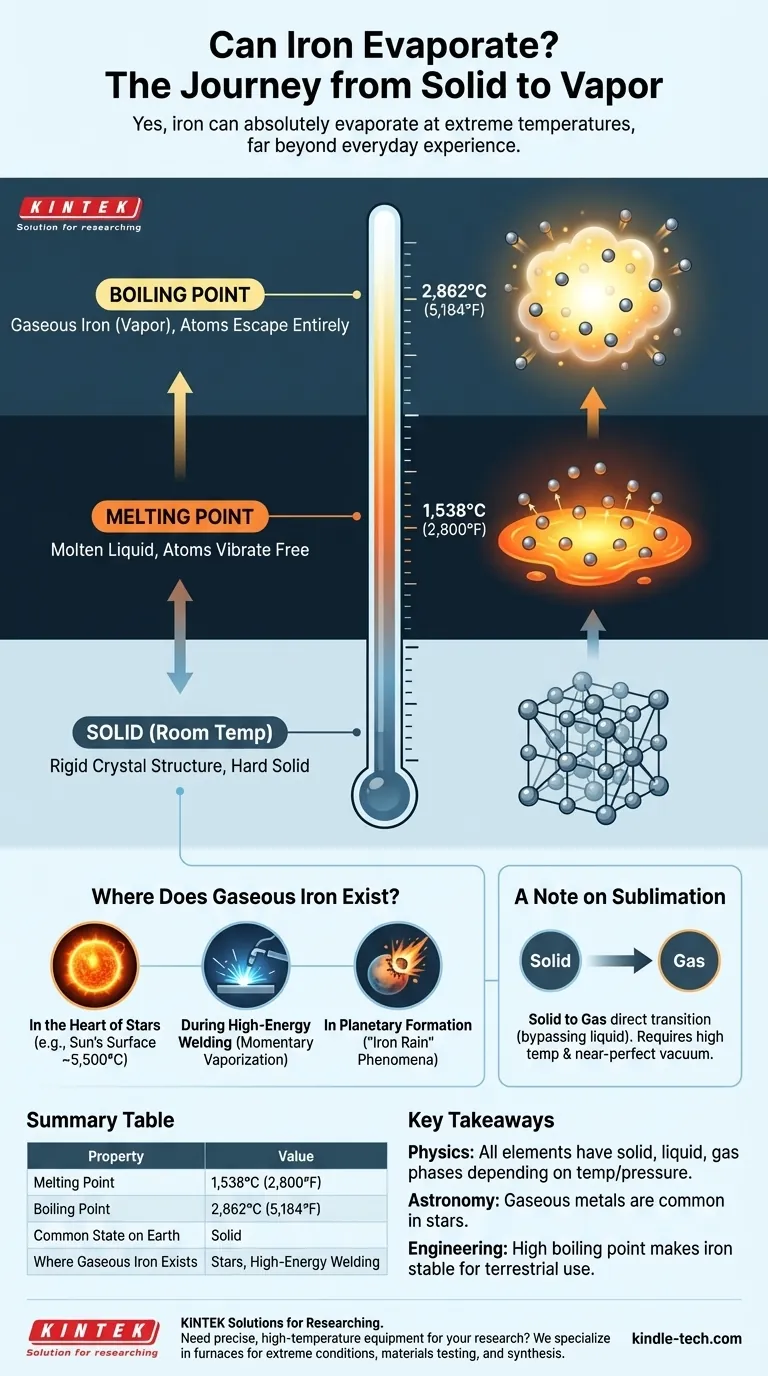
Sim, o ferro pode absolutamente evaporar. Como praticamente toda a matéria, o ferro pode existir como sólido, líquido e gás. No entanto, as condições necessárias para transformar ferro sólido em gás, ou vapor, envolvem temperaturas tão extremas que estão muito além do reino da experiência humana cotidiana.
O princípio central é que qualquer elemento fará a transição para um gás se for aquecido até seu ponto de ebulição. Para o ferro, essa temperatura é incrivelmente alta, 2.862°C (5.184°F), razão pela qual o percebemos como um material permanentemente sólido em todas as condições normais.

Compreendendo a Jornada para o Vapor de Ferro
Para entender como o ferro evapora, é melhor pensar no mesmo processo que a água passa, mas em uma escala de temperatura muito mais alta. O estado de qualquer matéria — sólido, líquido ou gás — é determinado pela energia e movimento de seus átomos.
Primeiro Passo: Do Sólido ao Líquido
Antes que o ferro possa ferver, ele deve primeiro derreter. À temperatura ambiente, os átomos de ferro estão presos em uma estrutura cristalina rígida, o que o torna um sólido duro.
À medida que você adiciona calor imenso, os átomos vibram cada vez mais violentamente até se libertarem dessa estrutura. Isso acontece no ponto de fusão do ferro de 1.538°C (2.800°F), transformando-o em um líquido fundido.
Segundo Passo: Do Líquido ao Gás
Para evaporar, ou ferver, os átomos de ferro precisam de ainda mais energia para superar completamente as forças que os mantêm unidos como um líquido.
Quando a temperatura atinge o ponto de ebulição do ferro de 2.862°C (5.184°F), os átomos escapam completamente, formando uma nuvem superaquecida de átomos de ferro individuais. Este é o vapor de ferro, ou ferro gasoso.
Onde o Ferro Gasoso Realmente Existe?
Embora você nunca veja uma poça de ferro evaporando em um dia quente, esse processo é comum em certos ambientes extremos no universo e em aplicações industriais especializadas.
No Coração das Estrelas
O lugar mais comum para encontrar ferro gasoso é dentro das estrelas, incluindo o nosso Sol. A superfície do Sol está a cerca de 5.500°C (9.940°F), bem acima do ponto de ebulição do ferro. Aqui, o ferro existe como um componente do plasma solar.
Durante a Soldagem de Alta Energia
Em uma escala muito menor e mais controlada, o calor intenso de um arco de soldagem industrial pode vaporizar momentaneamente uma pequena quantidade do metal que está sendo soldado. Este vapor de ferro esfria imediatamente e se ressolidifica como parte da solda.
Na Formação Planetária
Durante a formação do nosso sistema solar, impactos massivos entre corpos celestes teriam gerado energia suficiente para vaporizar rocha e ferro. Isso poderia ter levado a fenômenos como a "chuva de ferro" em protoplanetas à medida que o vapor esfriava e condensava.
Uma Nota sobre a Sublimação
Existe outro caminho para um estado gasoso chamado sublimação, onde um material se transforma diretamente de sólido para gás, ignorando completamente a fase líquida. É o que o gelo seco (dióxido de carbono sólido) faz à temperatura ambiente.
Teoricamente, o ferro também pode sublimar. No entanto, isso exigiria uma combinação de temperaturas muito altas e pressão extremamente baixa (um vácuo quase perfeito). Sob qualquer pressão atmosférica normal, a taxa de sublimação para o ferro é praticamente zero.
Principais Conclusões para a Compreensão da Matéria
- Se o seu foco principal é a física básica: Lembre-se de que todos os elementos podem existir nas fases sólida, líquida e gasosa; é apenas uma questão de atingir a temperatura e pressão certas.
- Se você está interessado em astronomia: Reconheça que metais gasosos, incluindo o ferro, são um componente comum e importante das estrelas e desempenham um papel fundamental em eventos cósmicos.
- Se você está pensando em engenharia: Aprecie que o ponto de ebulição incrivelmente alto do ferro é a propriedade fundamental que o torna um material estável e confiável para quase todas as aplicações terrestres.
Em última análise, saber que mesmo algo tão forte quanto o ferro pode ser transformado em gás reforça as leis físicas universais que governam toda a matéria.
Tabela Resumo:
| Propriedade | Valor |
|---|---|
| Ponto de Fusão | 1.538°C (2.800°F) |
| Ponto de Ebulição | 2.862°C (5.184°F) |
| Estado Comum na Terra | Sólido |
| Onde o Ferro Gasoso Existe | Estrelas, Soldagem de Alta Energia |
Precisa de equipamentos de alta temperatura precisos para sua pesquisa ou processos industriais? A KINTEK é especializada em equipamentos e consumíveis de laboratório, incluindo fornos que podem lidar com condições extremas para testes e síntese de materiais. Quer você esteja estudando transições de fase ou desenvolvendo novas ligas, nossas soluções confiáveis ajudam você a obter resultados precisos e repetíveis. Entre em contato com nossos especialistas hoje para discutir como podemos apoiar as necessidades de alta temperatura do seu laboratório!
Guia Visual