Em essência, a calcinação é um processo de purificação térmica. Envolve aquecer um material sólido a uma temperatura elevada, mas abaixo do seu ponto de fusão, numa atmosfera controlada com pouco ou nenhum ar. Este aquecimento preciso elimina substâncias voláteis como água e dióxido de carbono, desencadeia a decomposição química ou altera a estrutura cristalina interna do material, resultando num sólido mais puro, mais estável ou mais reativo.
O objetivo central da calcinação não é derreter um material, mas transformá-lo. Ao controlar cuidadosamente o calor e a atmosfera, pode remover seletivamente componentes indesejados ou alterar as propriedades de um material sem alterar o seu estado sólido.

Como a Calcinação Funciona Fundamentalmente
Para compreender a calcinação, é essencial entender seus três componentes principais: calor controlado, uma atmosfera específica e as mudanças químicas resultantes.
O Papel do Calor (Abaixo do Ponto de Fusão)
O parâmetro mais crítico na calcinação é a temperatura. O material é aquecido intensamente, mas sempre mantido abaixo do seu ponto de fusão.
Isso garante que o processo se concentre na decomposição química em vez de uma mudança de estado (de sólido para líquido). Permite a quebra controlada de compostos dentro da estrutura sólida.
A Atmosfera Controlada
A calcinação é tipicamente realizada na ausência ou com um fornecimento limitado de ar (oxigénio).
Esta é uma distinção crucial. Ao limitar o oxigénio, evita a oxidação ou combustão. O objetivo é decompor o material apenas com calor (decomposição térmica), e não fazê-lo reagir com oxigénio.
O Objetivo Principal: Decomposição
O calor aplicado durante a calcinação fornece a energia necessária para quebrar as ligações químicas. Isto é conhecido como decomposição térmica.
Um exemplo clássico é a produção de cal a partir de calcário. Quando o calcário (carbonato de cálcio, CaCO₃) é calcinado, decompõe-se em cal (óxido de cálcio, CaO) e liberta gás dióxido de carbono (CO₂), um componente volátil.
Principais Resultados da Calcinação
Dependendo do material e do objetivo, a calcinação alcança vários resultados específicos.
Remoção de Impurezas Voláteis
A aplicação mais comum é a purificação. O processo elimina substâncias voláteis, que são componentes que se transformam facilmente em gás quando aquecidos.
Isto inclui água ligada fisicamente (secagem), água ligada quimicamente em hidratos (desidratação) e dióxido de carbono de minérios de carbonato (descarbonatação). O resultado é uma versão mais concentrada e purificada do material base.
Indução de Transições de Fase
Às vezes, o objetivo não é remover nada, mas sim alterar a forma interna do material.
A calcinação pode induzir uma transição de fase, que altera a estrutura cristalina do material. Isso pode mudar as suas propriedades, como dureza, densidade ou reatividade, tornando-o adequado para uma aplicação específica, como um catalisador ou pigmento.
Preparação de Materiais para Processamento Posterior
Muitas vezes, a calcinação é uma etapa preparatória. Ao remover impurezas e criar uma substância mais reativa (como um óxido), o material é preparado para um processo subsequente.
Por exemplo, calcinar um minério pode tornar a extração subsequente do metal final por fundição mais eficiente e menos intensiva em energia.
Compreendendo as Compensações e Distinções
A calcinação é frequentemente confundida com outros processos térmicos. Entender as diferenças é fundamental para compreender a sua função específica.
Calcinação vs. Torrefação (Roasting)
A torrefação é outro processo térmico, mas é realizada com um excesso de ar. O seu objetivo é causar oxidação intencional. Por exemplo, converter um minério de sulfeto metálico em um óxido metálico. A calcinação, em contraste, evita ativamente a oxidação.
Calcinação vs. Sinterização
A sinterização também usa calor abaixo do ponto de fusão, mas o seu objetivo é totalmente diferente. A sinterização visa fundir pequenas partículas juntas para aumentar a densidade e a resistência do material. A calcinação purifica e decompõe; a sinterização consolida. Em muitos fluxos de trabalho industriais, a calcinação é realizada primeiro, seguida pela sinterização.
O Risco de Sobre-aquecimento
Controlar a temperatura é fundamental. Se o material for aquecido além do seu ponto de fusão, o processo deixa de ser calcinação. Torna-se fusão ou sinterização, o que pode ser indesejável e levar a um produto final completamente diferente e muitas vezes inutilizável.
Fazendo a Escolha Certa para o Seu Objetivo
A calcinação é uma ferramenta precisa usada para alcançar transformações específicas de materiais. O seu objetivo dita a sua aplicação.
- Se o seu foco principal é purificar um minério: Use a calcinação para eliminar água e carbonatos, criando um óxido mais concentrado antes da fundição.
- Se o seu foco principal é produzir cimento: A calcinação do calcário para produzir cal é a primeira etapa fundamental e inegociável do processo.
- Se o seu foco principal é ativar um catalisador: Use a calcinação para alcançar a estrutura cristalina ideal e a área de superfície necessárias para alta reatividade química.
Em última análise, a calcinação é uma técnica fundamental na ciência dos materiais para modificar deliberadamente a composição química e a estrutura de um sólido através do calor.
Tabela de Resumo:
| Aspeto Chave | Descrição |
|---|---|
| Objetivo Principal | Decomposição térmica e purificação sem fusão |
| Temperatura | Aquecido abaixo do ponto de fusão do material |
| Atmosfera | Ar/oxigénio limitado ou inexistente para prevenir a oxidação |
| Entradas Comuns | Calcário (CaCO₃), minérios, hidratos |
| Saídas Comuns | Cal (CaO), óxidos purificados, catalisadores ativados |
| Aplicações Chave | Produção de cimento, processamento de minério metálico, ativação de catalisadores |
Pronto para transformar os seus materiais com precisão?
O processo de calcinação é fundamental para purificar minérios, produzir cimento e ativar catalisadores. A KINTEK especializa-se no equipamento de laboratório de alta temperatura necessário para alcançar estas transformações térmicas precisas de forma fiável e eficiente.
Quer esteja a processar minerais ou a desenvolver materiais avançados, a nossa experiência em fornos de laboratório e consumíveis garante que tem as ferramentas certas para a decomposição controlada e transições de fase.
Contacte os nossos especialistas em processamento térmico hoje mesmo para discutir como as soluções KINTEK podem otimizar o seu fluxo de trabalho de calcinação e melhorar os resultados dos seus materiais.
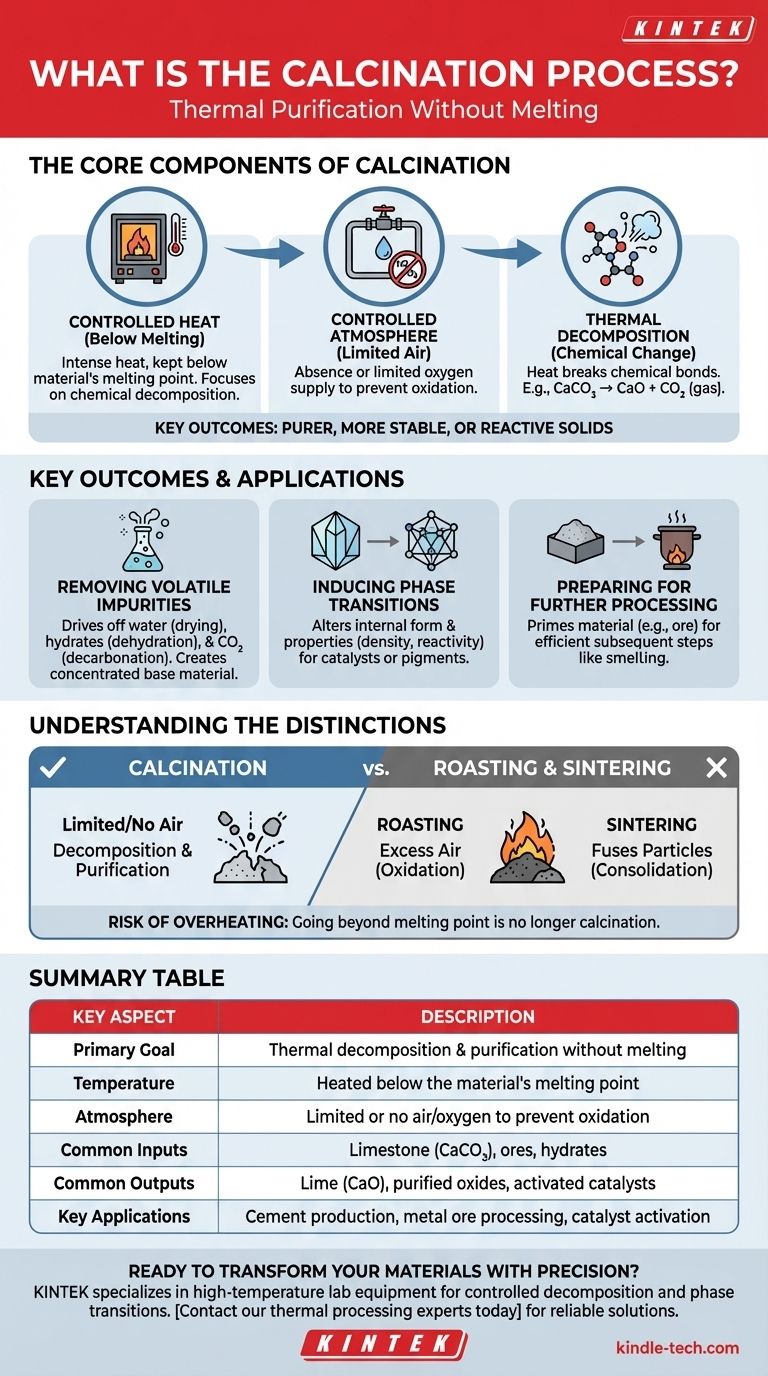
Guia Visual
Produtos relacionados
- Máquina de Forno de Pirólise de Forno Rotativo Elétrico Calciner Forno Rotativo Pequeno
- Forno Rotativo Elétrico de Trabalho Contínuo, Pequeno Forno Rotativo, Planta de Pirólise de Aquecimento
- Forno Vertical de Grafitação a Vácuo de Alta Temperatura
- Forno de Grafitação de Filme de Alta Condutividade Térmica de Grafite
- Forno de Grafitação a Vácuo de Ultra-Alta Temperatura de Grafite
As pessoas também perguntam
- Quais são os diferentes tipos de calcinadores? Um Guia para Selecionar o Equipamento de Processamento Térmico Correto
- Como os fornos rotativos são aquecidos? Métodos de Aquecimento Direto vs. Indireto Explicados
- O que é um forno elétrico de forno rotativo? Obtenha Aquecimento Uniforme Superior para Seus Materiais
- Quais são as vantagens do forno de forno rotativo? Obtenha Uniformidade e Eficiência Superiores
- A que temperatura ocorre a pirólise? Um Guia para Controlar a Produção do Seu Produto



















