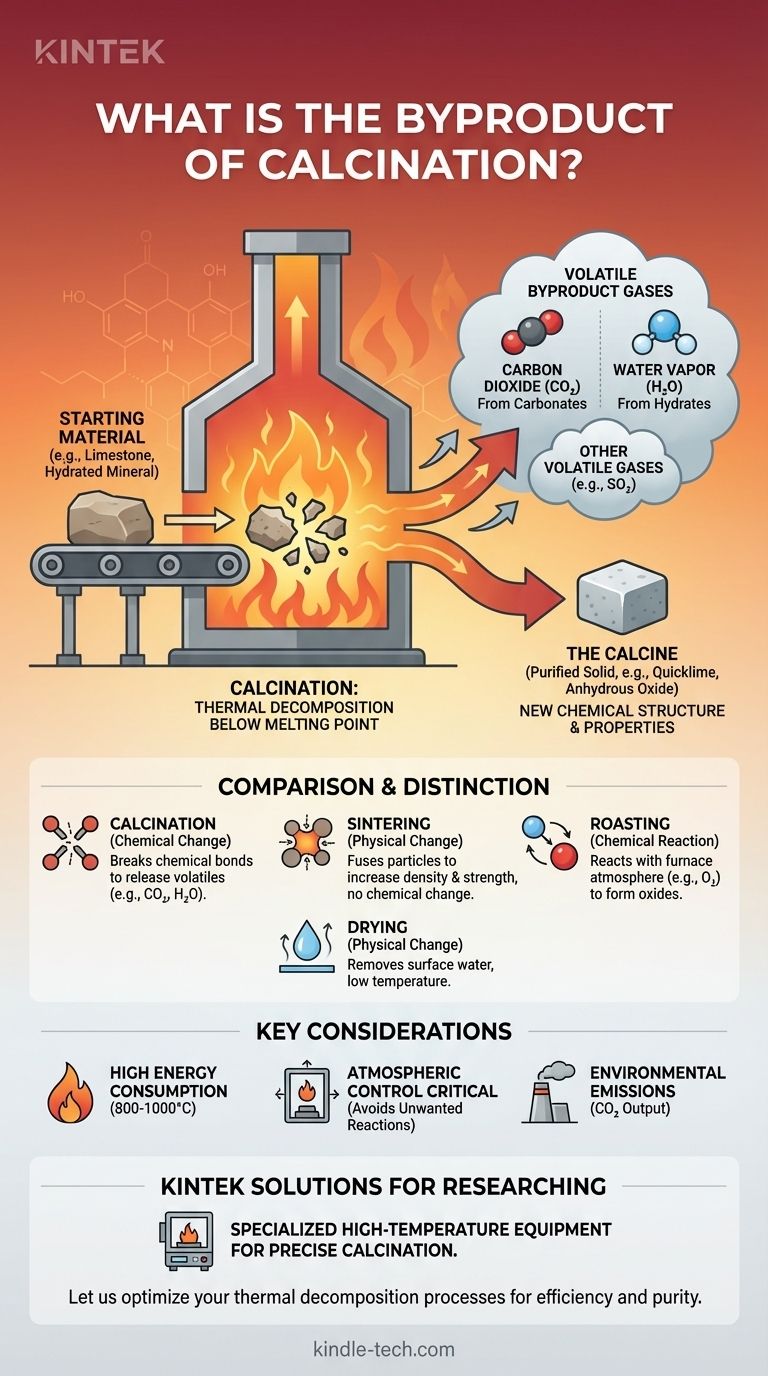
Na quase totalidade dos casos, o principal subproduto da calcinação é um gás. Este é mais comumente o dióxido de carbono (CO2) ao aquecer carbonatos como o calcário, ou vapor de água (H2O) ao aquecer minerais hidratados. O processo é uma forma de decomposição térmica, onde o calor intenso decompõe um composto em um sólido purificado e gases voláteis que são expelidos.
A calcinação é um processo de transformação química, não simplesmente de purificação. Utiliza calor elevado abaixo do ponto de fusão para decompor um material, alterando fundamentalmente sua estrutura química ao expelir subprodutos voláteis como dióxido de carbono ou vapor de água.

O que é Calcinação? Uma Análise Mais Profunda
A calcinação é um processo fundamental na metalurgia e na ciência dos materiais, particularmente na produção de cimento, cal e no refino de certos minérios. Compreender o mecanismo é fundamental para entender seu propósito.
O Princípio Central: Decomposição Térmica
Em sua essência, a calcinação trata da quebra de ligações químicas com calor. A energia aplicada faz com que o material de partida se decomponha em duas ou mais substâncias novas.
Uma dessas substâncias é o produto sólido desejado, frequentemente chamado de "calcinado". As outras substâncias são os subprodutos gasosos que são removidos.
Subprodutos Comuns Explicados
O subproduto específico depende inteiramente da composição química do material que está sendo aquecido.
- Dióxido de Carbono (CO2): Este é o exemplo mais famoso. Quando o carbonato de cálcio (CaCO3, calcário) é calcinado, ele se decompõe em óxido de cálcio (CaO, cal viva) e libera gás CO2. Esta é a reação central na fabricação de cimento.
- Vapor de Água (H2O): Muitos minerais existem como hidratos, o que significa que possuem moléculas de água presas em sua estrutura cristalina. A calcinação da bauxita (minério de alumínio) ou do gesso remove essa água quimicamente ligada como vapor.
- Outros Gases Voláteis: Em aplicações mais específicas, outros gases podem ser liberados. Por exemplo, o aquecimento de certos sulfatos pode liberar dióxido de enxofre (SO2), embora este processo frequentemente se sobreponha a uma técnica relacionada chamada ustulação.
O Produto Desejado: O Calcinado
O material sólido que resta após a remoção dos subprodutos voláteis é o objetivo principal. Este calcinado resultante agora possui diferentes propriedades químicas e físicas.
Por exemplo, a cal viva produzida a partir da calcinação do calcário é altamente reativa, o que é essencial para a fabricação de cimento e outros produtos químicos industriais.
Como a Calcinação Difere de Outros Tratamentos Térmicos
O termo "calcinação" é frequentemente confundido com outros processos de alta temperatura. A distinção reside no objetivo químico ou físico subjacente.
Calcinação vs. Sinterização
A calcinação altera a composição química de um material. Ela decompõe um composto em outro, removendo componentes voláteis.
A sinterização, como a referência observa corretamente, altera a forma física de um material. Ela usa calor para fundir pequenas partículas em uma única peça sólida sem derretê-las, aumentando sua resistência e densidade. A composição química permanece inalterada.
Calcinação vs. Ustulação (Roasting)
Este é um ponto de confusão muito comum. A calcinação é tipicamente realizada em uma atmosfera controlada ou inerte para causar a decomposição.
A ustulação, por outro lado, é um processo que envolve uma reação química com a atmosfera do forno, especificamente com oxigênio. É uma forma de oxidação, frequentemente usada para converter minérios de sulfeto metálico em óxidos metálicos.
Calcinação vs. Secagem
A secagem é um processo de baixa temperatura que remove a água fisicamente absorvida da superfície de uma substância.
A calcinação é um processo de alta temperatura que remove a água quimicamente ligada ou outros compostos voláteis de dentro da estrutura cristalina do material, exigindo significativamente mais energia para quebrar essas ligações químicas.
Compreendendo as Armadilhas e o Contexto
Embora poderosa, a calcinação é um processo industrial com considerações operacionais significativas que devem ser gerenciadas.
Alto Consumo de Energia
Atingir e manter as altas temperaturas necessárias para quebrar as ligações químicas (frequentemente 800-1000°C ou mais) torna a calcinação um processo extremamente intensivo em energia e custoso.
O Controle da Atmosfera é Crucial
A composição do gás dentro do forno é fundamental. Reações indesejadas, como a oxidação devido ao excesso de ar, podem ocorrer se a atmosfera não for cuidadosamente controlada, resultando em um produto final impuro.
Emissões Ambientais
Os subprodutos gasosos são uma saída primária. A calcinação do calcário para a produção de cimento é uma das maiores fontes industriais singulares de emissões globais de CO2, um fator crítico na gestão e regulamentação ambiental.
Fazendo a Escolha Certa para o Seu Objetivo
Compreender a calcinação permite reconhecer seu papel específico na criação dos materiais que moldam nosso mundo.
- Se o seu foco principal é a produção de cimento ou cal: A calcinação é o processo central usado para decompor o calcário (CaCO3) em cal viva reativa (CaO) ao expelir CO2.
- Se o seu foco principal é preparar um catalisador ou adsorvente: A calcinação é usada para remover água e precursores voláteis, criando um material puro e de alta área superficial pronto para uso.
- Se o seu foco principal é fortalecer uma peça de cerâmica ou pó metálico: Você está pensando em sinterização, que compacta partículas para aumentar a densidade, e não em calcinação, que altera sua química.
Em última análise, a calcinação é uma ferramenta fundamental para alterar quimicamente um material sólido usando calor para liberar seus componentes voláteis.
Tabela de Resumo:
| Material Calcinado | Gás Subproduto Comum | Produto Sólido Principal |
|---|---|---|
| Calcário (CaCO₃) | Dióxido de Carbono (CO₂) | Cal Viva (CaO) |
| Minerais Hidratados (ex: Bauxita, Gesso) | Vapor de Água (H₂O) | Óxido Anidro |
| Certos Sulfatos | Dióxido de Enxofre (SO₂) | Óxido Metálico |
Precisa de processamento térmico preciso para seus materiais?
A calcinação é uma etapa crítica na produção de tudo, desde cimento a catalisadores. A KINTEK é especializada em equipamentos de laboratório de alta temperatura, incluindo fornos ideais para processos de calcinação controlada. Nossas soluções ajudam você a alcançar as transformações químicas exatas de que precisa, com foco na eficiência e pureza.
Se você está desenvolvendo novos materiais, refinando minérios ou preparando catalisadores, a experiência da KINTEK em equipamentos de laboratório pode apoiar sua P&D e controle de qualidade. Deixe-nos ajudá-lo a otimizar seus processos de decomposição térmica.
Entre em contato com a KINTEK hoje para discutir suas necessidades específicas de calcinação e descobrir o equipamento certo para o seu laboratório.
Guia Visual