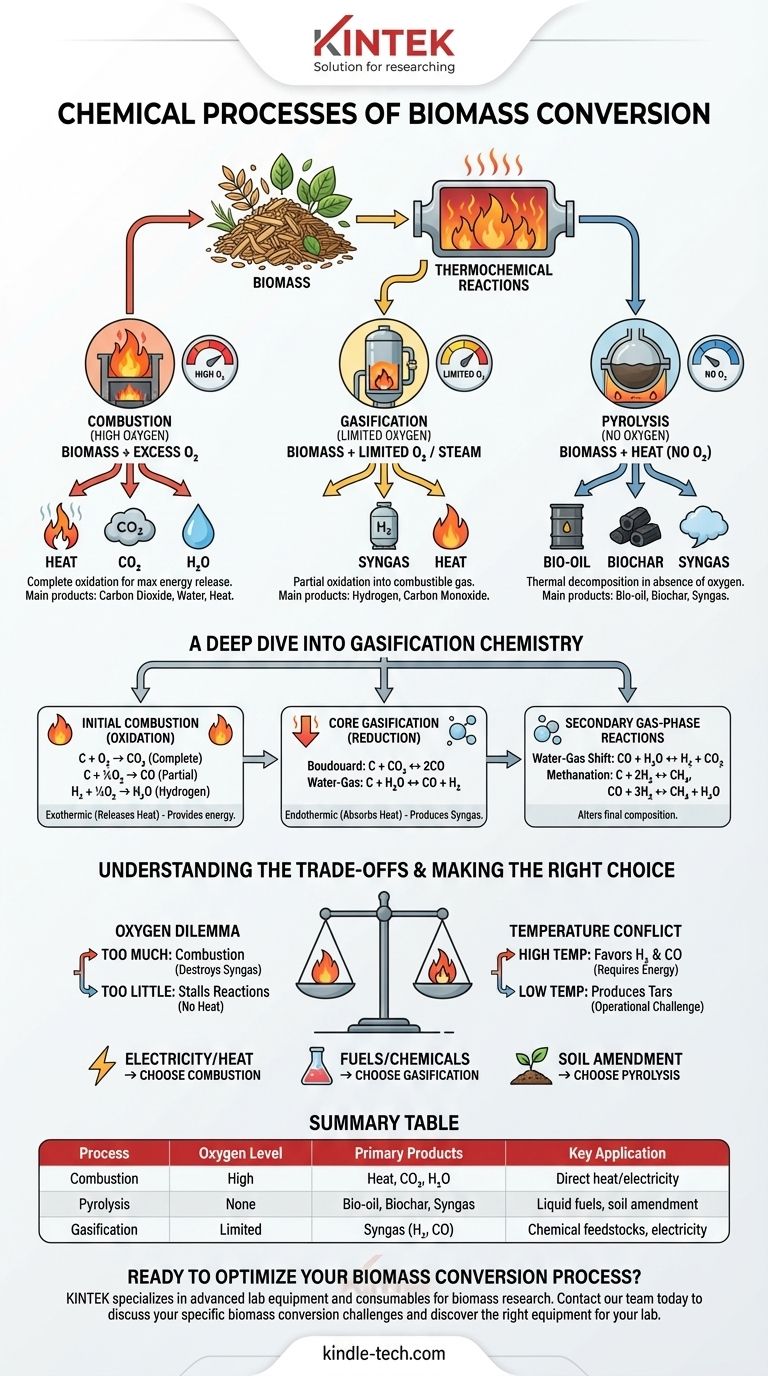
Em sua essência, a conversão de biomassa depende de uma série de reações termoquímicas controladas para decompor a matéria orgânica complexa. Processos como gaseificação, pirólise e combustão manipulam a temperatura e o oxigênio para transformar a biomassa em produtos valiosos como gás de síntese (syngas), bio-óleo ou calor, impulsionados por reações fundamentais envolvendo carbono, hidrogênio e oxigênio.
O desafio central da conversão de biomassa não é apenas iniciar reações químicas, mas controlá-las com precisão. Ao gerenciar fatores como a temperatura e a quantidade de oxigênio, podemos direcionar o processo para favorecer a criação de combustíveis e produtos químicos valiosos em vez da simples combustão em calor e dióxido de carbono.

As Principais Vias Termoquímicas
Para entender a química, você deve primeiro entender os métodos primários. A principal diferença entre eles é a quantidade de oxigênio fornecida ao processo, que dita os produtos finais.
Combustão (Alto Oxigênio)
A combustão é a oxidação completa da biomassa na presença de excesso de oxigênio.
Seu principal objetivo é liberar a quantidade máxima de energia na forma de calor. Este calor pode então ser usado para produzir vapor para geração de eletricidade ou para aplicações de aquecimento direto. Os principais produtos são dióxido de carbono (CO₂) e água (H₂O).
Pirólise (Sem Oxigênio)
A pirólise é a decomposição térmica da biomassa na ausência completa de oxigênio.
Em vez de queimar, a biomassa se decompõe em três produtos principais: um líquido conhecido como bio-óleo, um resíduo sólido chamado biocarvão e uma mistura gasosa conhecida como gás de síntese.
Gaseificação (Oxigênio Limitado)
A gaseificação é um processo de oxidação parcial que utiliza uma quantidade limitada e controlada de oxigênio ou vapor.
É projetada para converter biomassa sólida principalmente em uma mistura de gás combustível chamada gás de síntese, que é rica em hidrogênio (H₂) e monóxido de carbono (CO). Este gás de síntese é um intermediário versátil que pode ser queimado para gerar eletricidade ou usado como matéria-prima química.
Um Mergulho Profundo na Química da Gaseificação
A química da gaseificação é um processo de várias etapas onde a combustão inicial fornece a energia para reações subsequentes que produzem o gás de síntese desejado. As reações listadas abaixo frequentemente ocorrem simultaneamente em diferentes zonas de um gaseificador.
Etapa 1: Combustão Inicial (Oxidação)
O processo começa introduzindo uma pequena quantidade de oxigênio, o que inicia as reações de combustão. Estas são exotérmicas (liberam calor), fornecendo as altas temperaturas necessárias para o restante do processo.
C + O₂ → CO₂(Combustão Completa)C + ½O₂ → CO(Combustão Parcial)H₂ + ½O₂ → H₂O(Combustão de Hidrogênio)
Etapa 2: Gaseificação Central (Redução)
No ambiente de alta temperatura e pobre em oxigênio criado pela combustão inicial, o CO₂ quente e o vapor (H₂O) reagem com o carbono restante (carvão). Estas são as reações endotérmicas (absorvem calor) críticas que produzem o gás de síntese.
- Reação de Boudouard:
C + CO₂ ↔ 2CO - Reação de Gás de Água:
C + H₂O ↔ CO + H₂
Essas duas reações são o coração da conversão de carbono sólido em combustível gasoso valioso.
Etapa 3: Reações Secundárias na Fase Gasosa
Uma vez formado o gás de síntese inicial, ocorrem reações adicionais na fase gasosa que alteram sua composição final. Controlá-las ajuda a otimizar o gás para seu uso pretendido.
-
Reação de Deslocamento de Gás de Água:
CO + H₂O ↔ H₂ + CO₂Esta reação é crucial para ajustar a proporção hidrogênio-monóxido de carbono no gás de síntese final. -
Reações de Metanação:
C + 2H₂ ↔ CH₄CO + 3H₂ ↔ CH₄ + H₂OEssas reações produzem metano (CH₄), o que aumenta o poder calorífico do gás, mas pode ser indesejável se o objetivo for H₂ ou CO puro.
Compreendendo as Compensações
Gerenciar com sucesso um processo de conversão de biomassa é um ato de equilíbrio. As condições ideais dependem inteiramente do seu produto final desejado.
O Dilema do Oxigênio
A quantidade de oxigênio é o parâmetro de controle mais crítico. Muito oxigênio leva à combustão completa, liberando energia como calor, mas destruindo o valioso gás de síntese. Pouco oxigênio não produzirá calor suficiente, paralisando as reações de gaseificação endotérmicas.
O Conflito da Temperatura
Temperaturas mais altas (acima de 800°C) favorecem a produção de hidrogênio e monóxido de carbono via reações de Boudouard e Gás de Água. No entanto, manter essas altas temperaturas requer mais entrada de energia ou consome mais da matéria-prima para combustão.
O Papel da Umidade e do Alcatrão
A biomassa não é carbono puro. Seu teor de umidade alimenta diretamente as reações de Gás de Água e Deslocamento de Gás de Água, influenciando a proporção H₂/CO. A conversão incompleta, especialmente em temperaturas mais baixas, também pode produzir hidrocarbonetos complexos conhecidos como alcatrões, que podem entupir equipamentos e são um desafio operacional significativo.
Fazendo a Escolha Certa para o Seu Objetivo
A via química ideal depende inteiramente do que você deseja alcançar.
- Se o seu foco principal é gerar calor ou eletricidade diretamente: A combustão completa é o caminho mais direto, maximizando a liberação imediata de energia.
- Se o seu foco principal é criar combustíveis líquidos ou matérias-primas químicas: A gaseificação é superior, pois produz um intermediário de gás de síntese versátil que pode ser convertido cataliticamente em combustíveis (via Fischer-Tropsch) ou produtos químicos como metanol.
- Se o seu foco principal é produzir biocarvão para emenda do solo: A pirólise é o processo-alvo, pois maximiza o resíduo sólido de carvão, co-produzindo bio-óleo e gás.
Ao compreender essas vias químicas fundamentais, você pode controlar efetivamente a transformação da biomassa bruta em energia e produtos valiosos.
Tabela Resumo:
| Processo | Nível de Oxigênio | Produtos Primários | Aplicação Chave |
|---|---|---|---|
| Combustão | Alto | Calor, CO₂, H₂O | Calor/eletricidade direto |
| Pirólise | Nenhum | Bio-óleo, Biocarvão, Gás de Síntese | Combustíveis líquidos, emenda do solo |
| Gaseificação | Limitado | Gás de Síntese (H₂, CO) | Matérias-primas químicas, eletricidade |
Pronto para Otimizar Seu Processo de Conversão de Biomassa?
A KINTEK é especializada em equipamentos de laboratório avançados e consumíveis para pesquisa e desenvolvimento de biomassa. Seja você desenvolvendo catalisadores, analisando bio-óleo ou escalando reações de gaseificação, nossas ferramentas precisas ajudam você a controlar parâmetros críticos como temperatura e atmosfera. Deixe nossos especialistas apoiarem sua jornada da biomassa bruta a produtos energéticos valiosos.
Entre em contato com nossa equipe hoje para discutir seus desafios específicos de conversão de biomassa e descobrir o equipamento certo para seu laboratório.
Guia Visual
Produtos relacionados
- Forno Rotativo Elétrico Pequeno Forno de Pirólise de Biomassa
- Reatores de Laboratório Personalizáveis de Alta Temperatura e Alta Pressão para Diversas Aplicações Científicas
- Mini Reator Autoclave de Alta Pressão em Aço Inoxidável para Uso em Laboratório
- Reator Autoclave de Laboratório de Alta Pressão para Síntese Hidrotermal
- Reator Autoclavado de Alta Pressão em Aço Inoxidável Reator de Pressão Laboratorial
As pessoas também perguntam
- A que temperatura ocorre a pirólise? Um Guia para Controlar a Produção do Seu Produto
- Quais são os princípios de um forno rotativo? Domine a Mecânica do Processamento de Alta Temperatura
- Quais são as reações envolvidas na pirólise da biomassa? Desvende a Química para Bio-Produtos Personalizados
- Quais são as características dos modos de movimento de leito de escorregamento, desmoronamento e rolamento? Otimize seu processo rotativo
- Um forno rotativo é um forno? Descubra as Principais Diferenças para o Processamento Industrial







