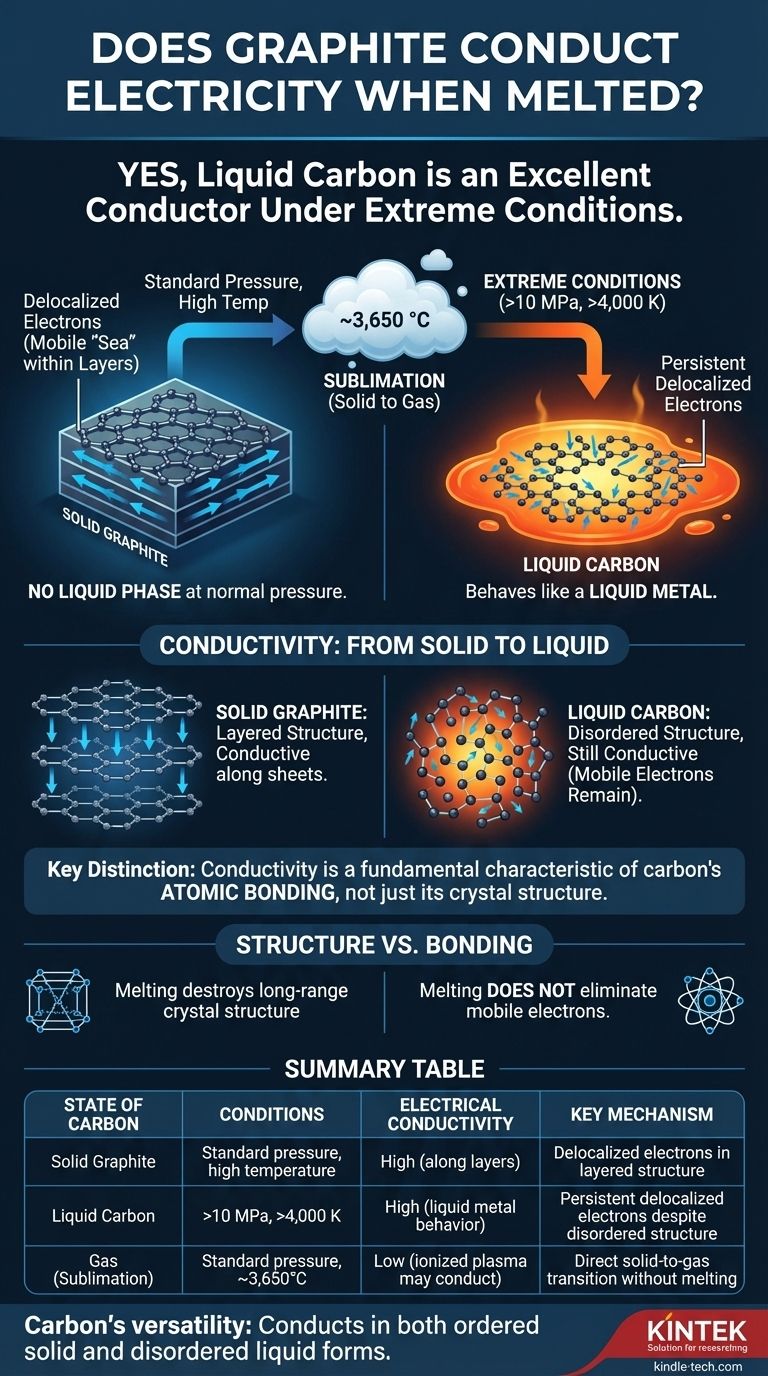
Sim, sob as condições extremas necessárias para derretê-lo, o carbono líquido é um excelente condutor elétrico. Embora o grafite não derreta sob pressão atmosférica normal, o carbono líquido que pode ser formado em pressões e temperaturas muito altas se comporta como um metal líquido, com elétrons livres para se mover e transportar uma corrente elétrica.
A questão não é simplesmente se o grafite fundido conduz eletricidade – ele conduz – mas por que. A resposta revela que a condutividade não é apenas uma propriedade da famosa estrutura em camadas do grafite, mas uma característica mais fundamental das ligações atômicas do carbono que persiste mesmo em um estado líquido desordenado.

O Desafio de Derreter o Grafite
Para entender a condução no carbono líquido, devemos primeiro apreciar o quão difícil é criá-lo. Para a maioria dos propósitos práticos, o grafite não possui uma fase líquida.
Sublimação, Não Fusão
À pressão atmosférica padrão, quando você aquece o grafite ao seu limite, ele não se transforma em líquido. Em vez disso, ele sublima – transformando-se diretamente de um sólido em um gás a temperaturas em torno de 3.650 °C (6.600 °F).
A Necessidade de Condições Extremas
Para forçar o carbono a um estado líquido, é preciso aplicar imensa pressão e temperatura simultaneamente. O carbono líquido só existe em pressões acima de 10 megapascais (~100 vezes a pressão atmosférica normal) e temperaturas que excedem 4.000 K (~3.727 °C ou 6.740 °F).
Condutividade: Do Sólido ao Líquido
A razão pela qual tanto o grafite sólido quanto o carbono líquido conduzem eletricidade reside na natureza única dos elétrons do carbono.
Como o Grafite Sólido Conduz
No grafite sólido, os átomos de carbono são arranjados em folhas planas e hexagonais. Cada átomo de carbono forma ligações fortes com três vizinhos, deixando seu quarto elétron externo deslocalizado.
Esses elétrons deslocalizados não estão ligados a nenhum átomo individual. Em vez disso, eles formam um "mar" móvel de elétrons dentro de cada folha, razão pela qual o grafite é um excelente condutor elétrico ao longo de suas camadas.
Condução no Estado Líquido
Quando o grafite é forçado a derreter, sua estrutura rígida e em camadas é destruída. Os átomos ficam desordenados e podem se mover livremente, como em qualquer líquido.
No entanto, o ambiente de ligação local ainda permite elétrons deslocalizados. O líquido é uma mistura complexa e flutuante de tipos de ligação, mas a presença de elétrons móveis persiste. Isso faz com que o carbono líquido se comporte como um metal líquido, com alta condutividade elétrica.
Compreendendo a Distinção Fundamental
É fácil supor que a condutividade do grafite é puramente resultado de sua estrutura em forma de folha. O comportamento do carbono líquido prova que esta é uma imagem incompleta.
Estrutura vs. Ligação
A principal conclusão é a diferença entre estrutura e ligação. Embora o derretimento destrua a estrutura cristalina de longo alcance do grafite, ele não elimina a ligação atômica fundamental que permite que os elétrons se tornem móveis.
Uma Limitação Prática
Este fenômeno é principalmente de interesse na física extrema e na ciência dos materiais. Na maioria das aplicações de engenharia, como em fornos de arco elétrico, você está lidando com um eletrodo de grafite sólido sublimando em um gás quente e ionizado (um plasma), e não em uma poça de carbono líquido.
Compreendendo as Propriedades do Carbono
Sua compreensão deste tópico depende do seu objetivo. Use estes pontos para enquadrar o conceito para o seu contexto específico.
- Se o seu foco principal é a química fundamental: A condutividade do carbono líquido demonstra que os elétrons deslocalizados, uma característica da ligação sp2 do carbono, não são perdidos quando a estrutura rígida da rede cristalina derrete.
- Se o seu foco principal é a engenharia prática: Para praticamente todas as aplicações, lembre-se de que o grafite sublimará em gás muito antes de ter a chance de derreter, um fator crítico para o projeto de sistemas de alta temperatura.
Em última análise, a capacidade do carbono de conduzir eletricidade em suas formas sólida ordenada e líquida desordenada revela a notável versatilidade de suas ligações atômicas.
Tabela Resumo:
| Estado do Carbono | Condições Necessárias | Condutividade Elétrica | Mecanismo Chave |
|---|---|---|---|
| Grafite Sólido | Pressão padrão, alta temperatura | Alta (ao longo das camadas) | Elétrons deslocalizados em estrutura em camadas |
| Carbono Líquido | >10 MPa, >4.000 K | Alta (comportamento de metal líquido) | Elétrons deslocalizados persistentes apesar da estrutura desordenada |
| Gás (Sublimação) | Pressão padrão, ~3.650°C | Baixa (plasma ionizado pode conduzir) | Transição direta de sólido para gás sem fusão |
Desbloqueie a Precisão na Pesquisa de Alta Temperatura com a KINTEK
Compreender comportamentos extremos de materiais, como a condutividade do carbono líquido, requer equipamentos de laboratório confiáveis. A KINTEK é especializada em fornos de laboratório de alto desempenho, eletrodos e consumíveis projetados para condições rigorosas. Seja você explorando a ciência dos materiais ou desenvolvendo sistemas de engenharia avançados, nossos produtos garantem precisão e durabilidade.
Pronto para aprimorar as capacidades do seu laboratório? Entre em contato conosco hoje para discutir como as soluções da KINTEK podem apoiar seus experimentos e objetivos de pesquisa em alta temperatura.
Guia Visual
Produtos relacionados
- Forno de Grafitação de Filme de Alta Condutividade Térmica de Grafite
- Eletrodo Eletroquímico de Grafite em Disco, Haste e Chapa
- Forno de Grafitação a Vácuo de Ultra-Alta Temperatura de Grafite
- Crisol de Grafite Puro de Alta Pureza para Evaporação
- Placa de Carbono Grafite Fabricada por Método de Prensagem Isostática
As pessoas também perguntam
- Que gás é usado no forno de grafite? Maximize a precisão com o gás inerte correto
- Quais são as desvantagens do forno de grafite? Limitações principais e custos operacionais
- Qual é a temperatura de um forno de grafite? Atinge calor extremo de até 3000 °C
- Quais são as interferências do forno de grafite? Supere Problemas de Matriz e Espectrais para GFAAS Preciso
- O que faz um forno de grafite? Atingir Calor Extremo e Análise Ultra-Sensível












