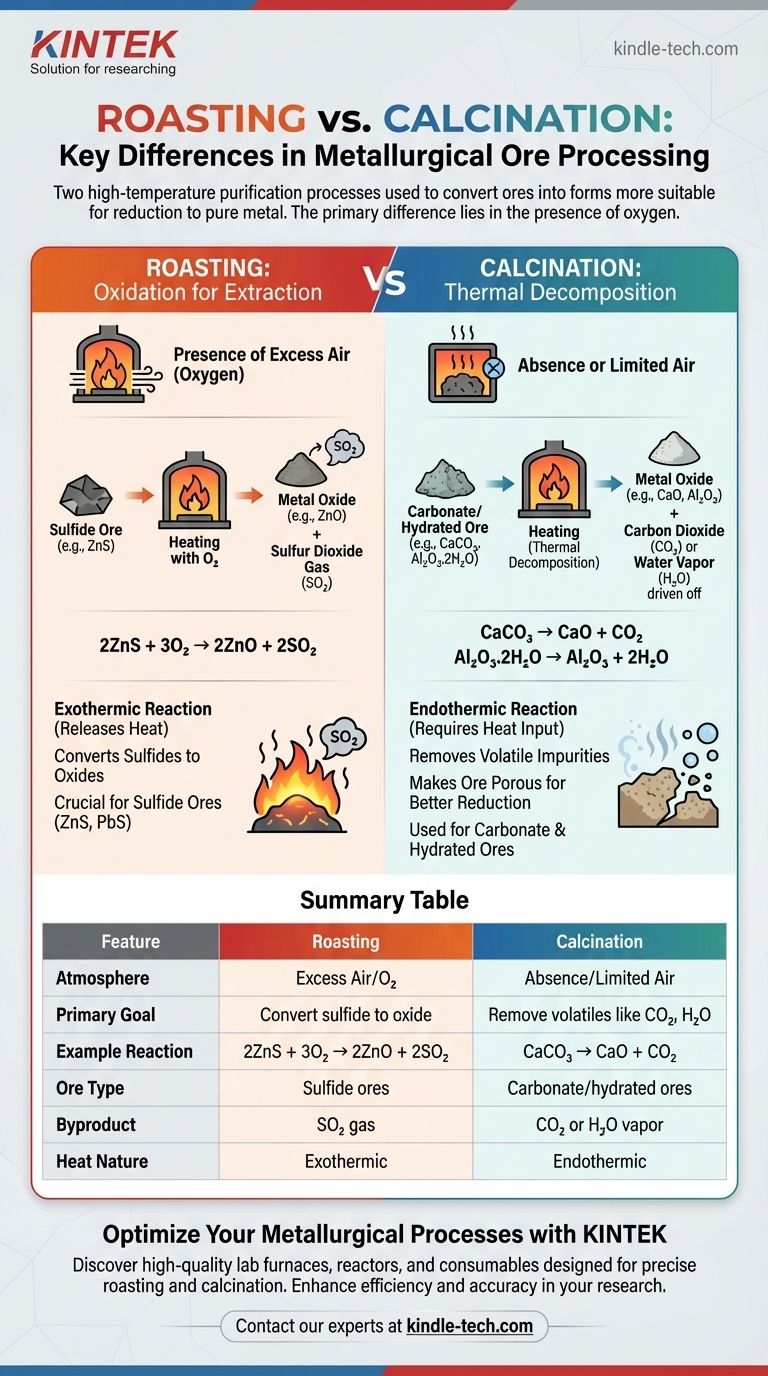
Em sua essência, a principal diferença entre ustulação e calcinação reside na presença de oxigênio. A ustulação é o processo de aquecer um minério concentrado a uma alta temperatura na presença de excesso de ar. Em contraste, a calcinação envolve o aquecimento de um minério a uma alta temperatura na ausência de ar ou com um suprimento muito limitado. Ambos são etapas preliminares cruciais na metalurgia, projetadas para converter minérios em uma forma mais adequada para a redução ao metal puro.
Embora ambos sejam processos de purificação de alta temperatura, a ustulação usa oxigênio para converter quimicamente minérios de sulfeto em óxidos. A calcinação, por outro lado, usa apenas calor para decompor termicamente minérios de carbonato ou hidratados, liberando substâncias voláteis como dióxido de carbono e água.

Compreendendo a Ustulação: Oxidação para Extração
A ustulação é um processo pirometalúrgico chave, o que significa que usa calor para provocar mudanças químicas em um minério. Sua principal aplicação é para minérios de sulfeto.
O Objetivo Fundamental
O principal objetivo da ustulação é converter um sulfeto metálico em um óxido metálico. Os óxidos metálicos são significativamente mais fáceis e economicamente mais viáveis de reduzir a um metal puro do que seus equivalentes de sulfeto.
A Reação Química e Exemplo
Durante a ustulação, o minério reage com o oxigênio do ar. Isso converte o sulfeto metálico em um óxido metálico e produz dióxido de enxofre (SO₂) gasoso como subproduto.
Um exemplo clássico é a ustulação da blenda de zinco (ZnS) para produzir óxido de zinco (ZnO), uma etapa crucial na extração de zinco:
2ZnS + 3O₂ → 2ZnO + 2SO₂
Características Principais da Ustulação
Este processo é realizado em um forno especializado, como um forno de reverberação ou flash, a uma temperatura abaixo do ponto de fusão do minério. Para muitos minérios de sulfeto, a reação é exotérmica, o que significa que libera calor e pode se sustentar uma vez iniciada.
Compreendendo a Calcinação: Decomposição Térmica
A calcinação é outro processo de tratamento térmico, mas seu mecanismo químico é totalmente diferente. É usada principalmente para minérios de carbonato e hidratados.
O Objetivo Fundamental
O objetivo da calcinação é remover impurezas voláteis aquecendo o minério. Isso libera substâncias como dióxido de carbono (de carbonatos) ou água (de óxidos hidratados), deixando um óxido metálico mais concentrado.
A Reação Química e Exemplo
A calcinação é uma reação de decomposição térmica que ocorre na ausência de ar. Um exemplo primário é a calcinação do calcário (carbonato de cálcio, CaCO₃) para produzir cal (óxido de cálcio, CaO):
CaCO₃ → CaO + CO₂
Outro uso comum é para minérios hidratados, como a bauxita (óxido de alumínio hidratado), para remover água antes do processo de extração de alumínio:
Al₂O₃.2H₂O → Al₂O₃ + 2H₂O
Características Principais da Calcinação
Este processo é endotérmico, exigindo um fornecimento contínuo de calor. Ele torna o minério poroso, o que aumenta a área de superfície disponível para a etapa de redução subsequente, aumentando assim sua eficiência.
Compreendendo as Vantagens e o Contexto
A escolha entre esses processos não é uma questão de preferência; é ditada pela química do minério. Entender o porquê é fundamental para compreender a metalurgia.
Por Que Não Reduzir Sulfetos Diretamente?
Reduzir sulfetos metálicos diretamente a metal é termodinamicamente difícil e caro. Convertê-los em óxidos primeiro oferece um caminho muito mais eficiente e econômico para a redução, tipicamente usando carbono (coque) como agente redutor.
Manuseando os Subprodutos
A ustulação produz dióxido de enxofre (SO₂), um gás que pode causar chuva ácida se liberado na atmosfera. As modernas plantas metalúrgicas capturam esse gás e o utilizam para fabricar ácido sulfúrico, transformando um potencial passivo ambiental em um valioso produto comercial.
A Importância de um Minério Poroso
A capacidade da calcinação de criar um minério poroso e quebradiço é uma vantagem significativa. Essa maior área de superfície permite que o agente redutor (como o monóxido de carbono em um alto-forno) interaja mais efetivamente com o óxido metálico, acelerando a extração final do metal.
Fazendo a Escolha Certa para o Seu Minério
A escolha entre ustulação e calcinação é ditada inteiramente pela composição química do minério que você precisa processar.
- Se o seu minério é um sulfeto (como blenda de zinco, ZnS, ou galena, PbS): Você deve usar a ustulação para converter o sulfeto em um óxido antes que ele possa ser reduzido ao metal puro.
- Se o seu minério é um carbonato (como calamina, ZnCO₃, ou calcário, CaCO₃): Você deve usar a calcinação para decompô-lo termicamente e liberar o dióxido de carbono, obtendo o óxido metálico.
- Se o seu minério é um óxido hidratado (como bauxita, Al₂O₃.2H₂O): Você deve usar a calcinação para remover a água quimicamente ligada e produzir um óxido puro e anidro.
Compreender essa distinção fundamental é o primeiro passo para projetar um processo de extração metalúrgica eficaz e eficiente.
Tabela Resumo:
| Característica | Ustulação | Calcinação |
|---|---|---|
| Atmosfera | Excesso de ar (presença de O₂) | Ausência ou ar limitado |
| Objetivo Principal | Converter minérios de sulfeto em óxidos | Remover impurezas voláteis (CO₂, H₂O) |
| Exemplo de Reação | 2ZnS + 3O₂ → 2ZnO + 2SO₂ | CaCO₃ → CaO + CO₂ |
| Tipo de Minério | Minérios de sulfeto (p. ex., ZnS, PbS) | Minérios de carbonato/hidratados (p. ex., CaCO₃, bauxita) |
| Subproduto | Gás SO₂ | Vapor de CO₂ ou H₂O |
| Natureza do Calor | Exotérmico (libera calor) | Endotérmico (requer entrada de calor) |
Otimize Seus Processos Metalúrgicos com a KINTEK
Seja você processando minérios de sulfeto por ustulação ou decompondo carbonatos por calcinação, ter o equipamento de laboratório certo é crucial para a eficiência e precisão. A KINTEK é especializada no fornecimento de fornos de laboratório, reatores e consumíveis de alta qualidade, projetados para atender às rigorosas demandas de testes e pesquisas metalúrgicas.
Nossos produtos garantem controle preciso de temperatura, aquecimento uniforme e durabilidade — fatores chave para operações bem-sucedidas de ustulação e calcinação. Ao fazer parceria com a KINTEK, você tem acesso a:
- Equipamentos confiáveis que aumentam a reprodutibilidade do processo
- Suporte especializado para ajudá-lo a selecionar as ferramentas certas para o seu tipo de minério específico
- Soluções que melhoram a segurança e a conformidade ambiental
Pronto para refinar seu processo de extração? Entre em contato com nossos especialistas hoje para discutir como os equipamentos de laboratório da KINTEK podem apoiar suas inovações metalúrgicas e impulsionar sua pesquisa.
Guia Visual