Em resumo, a calcinação do calcário produz dois produtos principais: óxido de cálcio (CaO) e dióxido de carbono (CO₂). Este processo envolve o aquecimento do calcário, que é primariamente carbonato de cálcio (CaCO₃), a uma alta temperatura, fazendo com que ele se decomponha quimicamente em vez de simplesmente derreter ou queimar.
A calcinação do calcário é um processo industrial fundamental. É uma reação de decomposição térmica que transforma uma rocha natural estável em um bloco de construção químico altamente reativo (óxido de cálcio) ao liberar gás dióxido de carbono.

A Química da Calcinação: Uma Análise Detalhada
Para compreender totalmente o processo, é essencial entender a transformação química subjacente e as condições necessárias para que ela ocorra.
A Equação Química Central
A reação é elegantemente simples e é um pilar da química inorgânica. É uma reação endotérmica, o que significa que requer uma entrada contínua de energia (calor) para prosseguir.
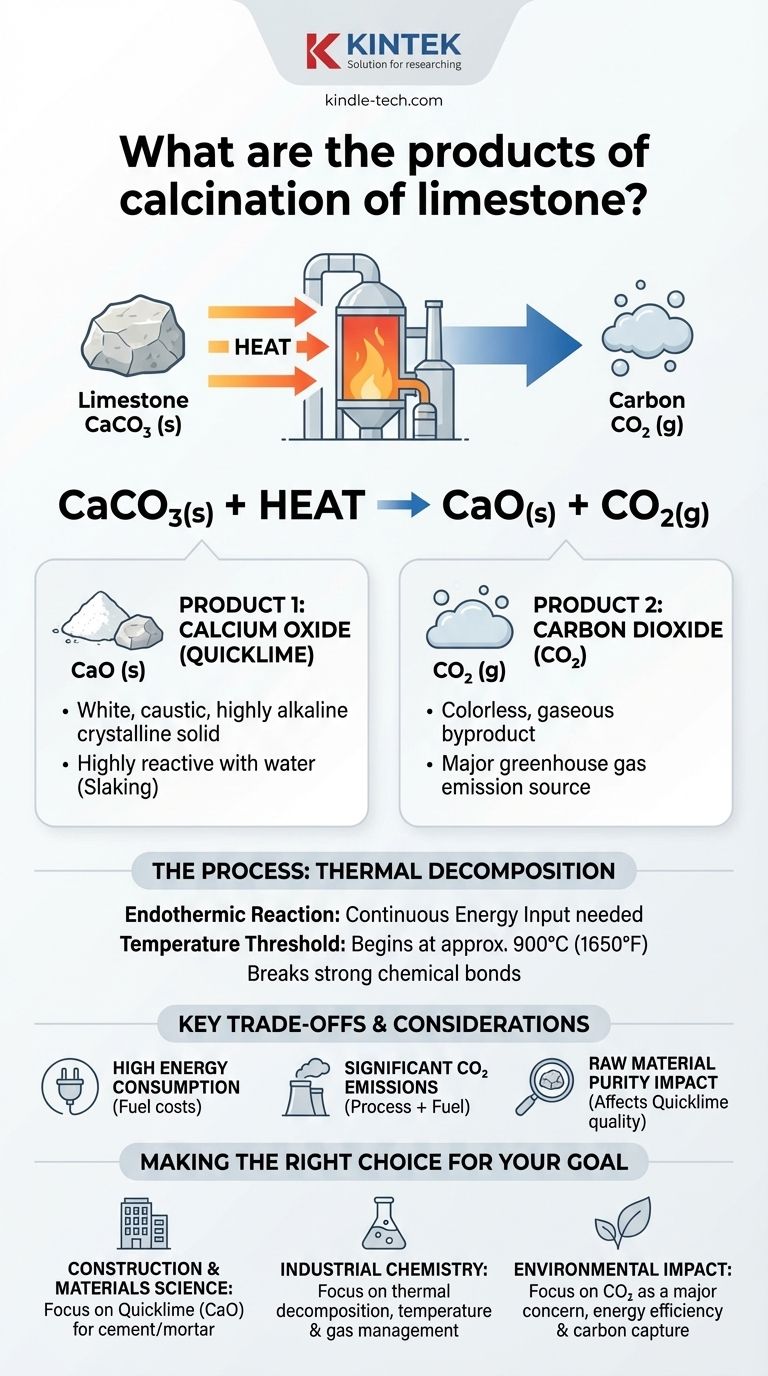
A equação balanceada é: CaCO₃(s) + Calor → CaO(s) + CO₂(g)
Isso mostra que uma molécula de carbonato de cálcio sólido se decompõe em uma molécula de óxido de cálcio sólido e uma molécula de dióxido de carbono gasoso.
O Papel da Decomposição Térmica
A calcinação não é uma reação *com* calor; é uma decomposição *causada* pelo calor. A energia térmica é usada para quebrar as fortes ligações químicas dentro da estrutura do carbonato de cálcio.
Limiar Crítico de Temperatura
A decomposição do carbonato de cálcio começa em aproximadamente 900°C (1650°F) sob pressão atmosférica normal. Em fornos industriais, as temperaturas são frequentemente mantidas mais altas para garantir que a reação prossiga de forma eficiente e completa.
Compreendendo os Produtos e Suas Propriedades
Os dois produtos desta reação têm características e usos vastamente diferentes, o que explica por que o processo é tão fundamental para a indústria.
Produto 1: Óxido de Cálcio (Cal Viva)
O óxido de cálcio, comumente conhecido como cal viva ou cal queimada, é o principal produto desejado. É um sólido cristalino branco, cáustico e altamente alcalino.
Sua propriedade mais importante é sua alta reatividade, especialmente com a água. Esta reação exotérmica, chamada hidratação, produz hidróxido de cálcio, ou cal hidratada.
Produto 2: Dióxido de Carbono (CO₂)
O dióxido de carbono é o subproduto gasoso que é liberado e removido do forno durante o processo.
Embora às vezes seja capturado para outros usos industriais, é mais frequentemente considerado um produto residual e uma fonte significativa de emissões de gases de efeito estufa.
Compreendendo as Compensações e Considerações Chave
Embora o processo seja quimicamente direto, sua aplicação industrial envolve desafios e impactos significativos que devem ser gerenciados.
Alto Consumo de Energia
Atingir e manter temperaturas acima de 900°C é um processo extremamente intensivo em energia. Os custos de combustível representam uma grande parte da despesa operacional da produção de cal viva.
Emissões Significativas de CO₂
A calcinação do calcário é uma grande fonte global de emissões de dióxido de carbono. O CO₂ provém de duas fontes: a decomposição química do calcário em si e os combustíveis fósseis tipicamente queimados para aquecer os fornos.
Impacto da Pureza da Matéria-Prima
A qualidade da cal viva final depende diretamente da pureza do calcário inicial. Impurezas como sílica, argila ou carbonato de magnésio podem afetar a reatividade e as propriedades do produto final, o que é crucial para aplicações como a fabricação de aço e cimento.
Fazendo a Escolha Certa para o Seu Objetivo
Compreender este processo permite que você aprecie seu papel em diferentes campos. A importância dos produtos depende inteiramente da sua aplicação específica.
- Se o seu foco principal for construção e ciência dos materiais: O produto chave é o óxido de cálcio (cal viva), pois é o precursor essencial para cimento e argamassa.
- Se o seu foco principal for química industrial: Veja isso como uma reação clássica de decomposição térmica onde gerenciar a temperatura, as entradas de energia e a remoção de gás são as variáveis críticas do processo.
- Se o seu foco principal for impacto ambiental: Reconheça que o subproduto, o dióxido de carbono, é uma grande preocupação, tornando a eficiência energética e as tecnologias de captura de carbono vitais para o futuro da indústria.
Em última análise, entender os produtos da calcinação do calcário é o primeiro passo para dominar sua aplicação em inúmeras indústrias essenciais.
Tabela de Resumo:
| Produto | Fórmula Química | Nome Comum | Propriedades Chave |
|---|---|---|---|
| Óxido de Cálcio | CaO | Cal Viva | Branco, cáustico, altamente alcalino, reativo com água |
| Dióxido de Carbono | CO₂ | - | Gás incolor, gás de efeito estufa, subproduto industrial |
Otimize seu processo de calcinação com os equipamentos de laboratório avançados da KINTEK. Quer você esteja pesquisando reações de decomposição térmica ou escalando a produção industrial, nossos fornos e calcinadores de alta temperatura garantem controle preciso de temperatura e eficiência energética. Fornecemos as ferramentas confiáveis que você precisa para produzir cal viva de alta pureza enquanto gerencia o consumo de energia e as emissões. Contate-nos hoje (#ContactForm) para discutir como nossas soluções podem aprimorar seus fluxos de trabalho de ciência dos materiais e química industrial.
Guia Visual
Produtos relacionados
- Forno Rotativo Elétrico de Trabalho Contínuo, Pequeno Forno Rotativo, Planta de Pirólise de Aquecimento
- Máquina de Forno de Pirólise de Forno Rotativo Elétrico Calciner Forno Rotativo Pequeno
As pessoas também perguntam
- Como os fornos rotativos são aquecidos? Métodos de Aquecimento Direto vs. Indireto Explicados
- Qual é a temperatura de um forno rotativo? Depende do seu material e objetivo do processo
- Um forno rotativo é um forno? Descubra as Principais Diferenças para o Processamento Industrial
- Qual é o processo do forno rotativo? Alcance a Transformação Precisa de Materiais Industriais
- A que temperatura ocorre a pirólise? Um Guia para Controlar a Produção do Seu Produto

