Sim, o grafite conduz eletricidade prontamente. É um dos poucos não-metais que é um condutor elétrico eficaz, uma propriedade que decorre diretamente de sua estrutura atômica única e do comportamento de seus elétrons.
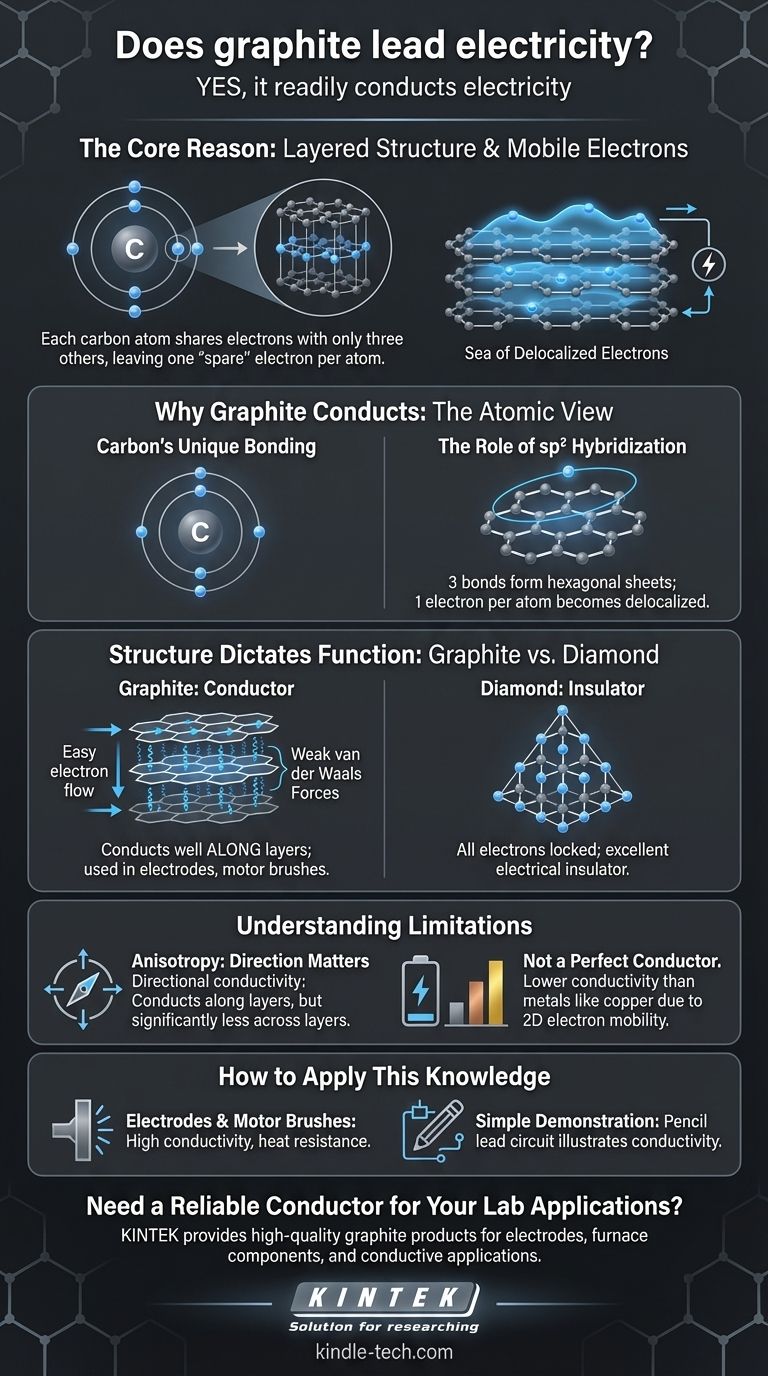
A razão central pela qual o grafite conduz eletricidade é sua estrutura em camadas. Cada átomo de carbono compartilha elétrons com apenas outros três átomos, deixando um elétron por átomo livre para se mover ao longo dessas camadas, criando um "mar" de elétrons móveis que podem transportar uma corrente elétrica.

Por que o Grafite Conduz Eletricidade: A Visão Atômica
Para entender a condutividade do grafite, devemos observar como seus átomos de carbono estão dispostos e ligados. A explicação reside em um conceito chamado deslocalização de elétrons.
A Ligação Única do Carbono
Um átomo de carbono tem quatro elétrons na camada externa (elétrons de valência) disponíveis para ligação. Em muitos compostos de carbono, como metano ou diamante, todos esses quatro elétrons formam ligações fortes e localizadas.
O Papel da Hibridização sp2
No grafite, no entanto, cada átomo de carbono usa apenas três de seus quatro elétrons de valência para formar fortes ligações covalentes com três átomos vizinhos. Este arranjo, conhecido como hibridização sp2, cria uma rede hexagonal plana, muito parecida com uma tela de galinheiro.
Um "Mar" de Elétrons Deslocalizados
Isso deixa um elétron por átomo de carbono não ligado. Esses elétrons "extras" não estão presos entre dois átomos específicos; em vez disso, eles se tornam deslocalizados, formando uma nuvem de elétrons de livre movimento por todo o plano da folha hexagonal. Quando uma voltagem é aplicada, esses elétrons móveis fluem, criando uma corrente elétrica.
Estrutura Determina a Função: Grafite vs. Diamante
O contraste entre grafite e diamante, ambas formas puras de carbono, fornece a ilustração mais clara de como a estrutura atômica determina as propriedades elétricas.
A Rede em Camadas do Grafite
O grafite é essencialmente folhas empilhadas dessas camadas hexagonais de carbono (agora conhecidas como grafeno). Os elétrons deslocalizados movem-se com facilidade ao longo dessas camadas, tornando o grafite altamente condutor nessa direção.
As próprias camadas são mantidas juntas por forças muito mais fracas (forças de van der Waals), razão pela qual o grafite parece escorregadio e é usado como lubrificante.
A Fortaleza Rígida do Diamante
Em um diamante, cada átomo de carbono usa todos os seus quatro elétrons de valência para se ligar a outros quatro átomos de carbono em uma rede tetraédrica tridimensional rígida. Isso é conhecido como hibridização sp3.
Como todos os elétrons estão presos em ligações covalentes fortes e localizadas, não há elétrons móveis para transportar uma corrente. Isso torna o diamante um excelente isolante elétrico.
Entendendo as Limitações
Embora o grafite seja um condutor, suas propriedades não são uniformes e ele não se comporta exatamente como um metal típico.
Anisotropia: A Direção Importa
O grafite é um condutor anisotrópico. Isso significa que sua condutividade é direcional. Ele conduz eletricidade extremamente bem ao longo de suas camadas, mas é significativamente menos condutor através das camadas. As ligações fracas entre as camadas atuam como uma barreira ao fluxo de elétrons.
Não é um Condutor Perfeito
Embora seja um bom condutor para um não-metal, sua condutividade é geralmente menor do que a de metais como cobre, prata ou ouro. Isso ocorre porque os metais têm um mar tridimensional de elétrons, enquanto a mobilidade dos elétrons do grafite é primariamente bidimensional.
Como Aplicar Este Conhecimento
Compreender as propriedades do grafite permite seu uso em uma ampla gama de aplicações, desde lápis do dia a dia até eletrônicos de alta tecnologia.
- Se seu foco principal é criar eletrodos ou escovas de motor: A combinação de alta condutividade, resistência ao calor e propriedades autolubrificantes do grafite o torna uma escolha ideal.
- Se seu foco principal for em materiais avançados: Reconheça que uma única camada de grafite é grafeno, um material com propriedades elétricas e mecânicas extraordinárias na escala nanométrica.
- Se seu foco principal for uma demonstração simples de condutividade: Um "grafite" de lápis comum (que é uma mistura de grafite e argila) pode ser usado para desenhar um circuito condutor no papel, ilustrando o princípio de forma segura e acessível.
Em última análise, o grafite é um exemplo perfeito de como o arranjo atômico de um material dita sua função no mundo real.
Tabela de Resumo:
| Propriedade | Grafite | Diamante |
|---|---|---|
| Condutividade Elétrica | Bom Condutor (ao longo das camadas) | Excelente Isolante |
| Ligação Atômica | Hibridização sp2 (3 ligações) | Hibridização sp3 (4 ligações) |
| Comportamento dos Elétrons | Elétrons deslocalizados movem-se ao longo das camadas | Todos os elétrons estão presos em ligações |
| Estrutura | Folhas hexagonais em camadas | Rede tetraédrica 3D rígida |
Precisa de um Condutor Confiável para Suas Aplicações de Laboratório?
As propriedades exclusivas do grafite o tornam um material essencial para eletrodos, componentes de fornos e outras aplicações condutoras de alta temperatura.
Na KINTEK, nos especializamos em fornecer equipamentos e consumíveis de laboratório de alta qualidade, incluindo produtos de grafite adaptados para atender às exigências rigorosas do seu laboratório. Nossa experiência garante que você obtenha os materiais certos para controle preciso de temperatura, aquecimento uniforme e desempenho duradouro.
Aumente a eficiência e a confiabilidade do seu laboratório — entre em contato com nossos especialistas hoje mesmo para encontrar a solução perfeita para suas necessidades!
Guia Visual
Produtos relacionados
- Eletrodo Eletroquímico de Grafite em Disco, Haste e Chapa
- Forno de Grafitação a Vácuo de Ultra-Alta Temperatura de Grafite
- Placa de Carbono Grafite Fabricada por Método de Prensagem Isostática
- Crisol de Grafite Puro de Alta Pureza para Evaporação
- Crisol de grafite puro de alta pureza para evaporação por feixe de elétrons
As pessoas também perguntam
- Qual é o procedimento correto para instalar e conectar um eletrodo de grafite durante um experimento? Garanta Resultados Eletroquímicos Precisos
- Por que os ânodos dimensionalmente estáveis (DSA) são preferidos para a eletroextração de índio? Garanta resultados de alta pureza.
- Quais são os procedimentos de manutenção padrão para eletrodos de grafite? Um Guia para Dados Eletroquímicos Confiáveis
- Por que os eletrodos de grafite são preferidos para reações eletroquímicas? Soluções Duráveis e de Baixo Custo para Depósitos Pesados
- Quais são as precauções essenciais para manusear eletrodos de grafite? Garanta a Segurança e Maximize o Desempenho











