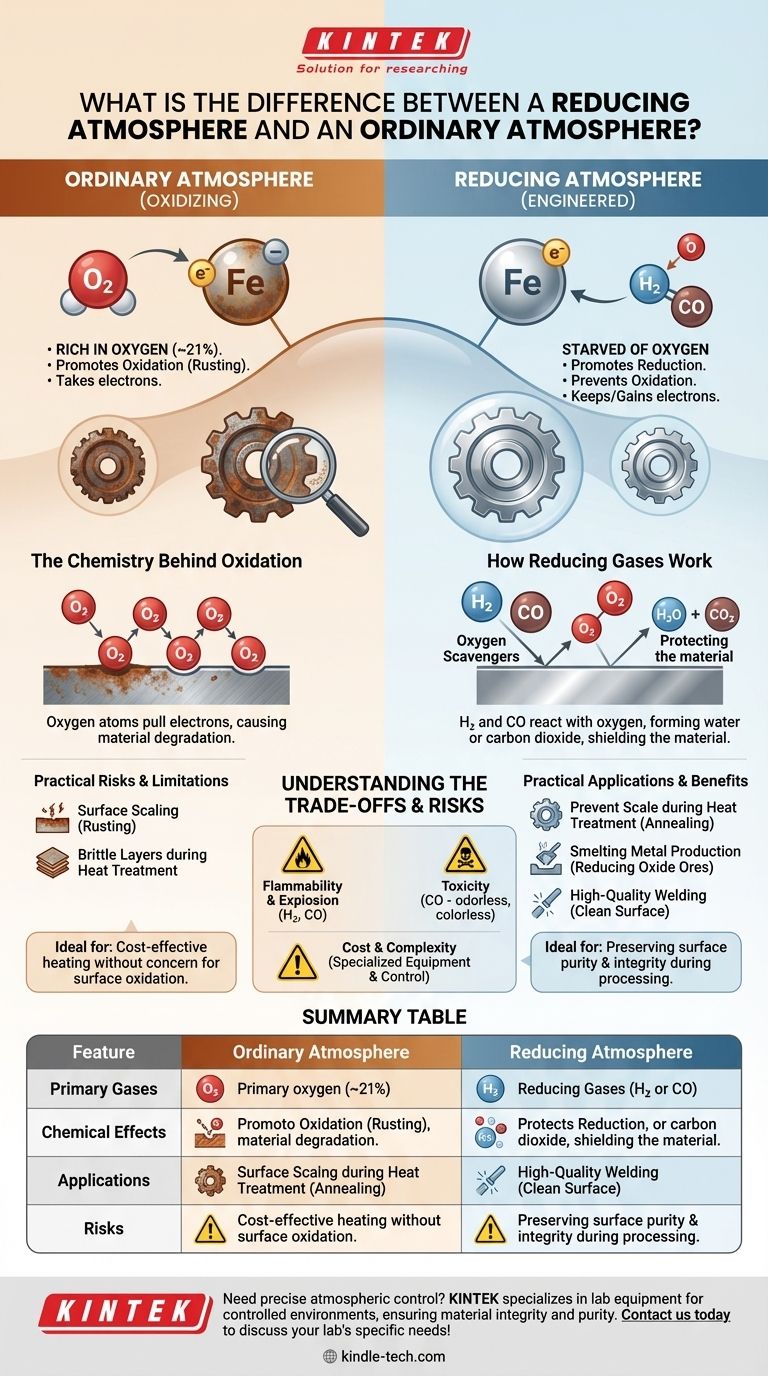
Em sua essência, a diferença reside na reatividade química. Uma atmosfera comum, rica em oxigênio, promove ativamente a oxidação — o processo responsável pela ferrugem e combustão. Uma atmosfera redutora é um ambiente projetado que faz o oposto; é privada de oxigênio e frequentemente contém gases específicos que previnem ou até revertem a oxidação, promovendo a redução química.
Uma atmosfera comum faz com que os materiais oxidem, tirando seus elétrons. Uma atmosfera redutora cria um ambiente químico que impede isso, forçando os materiais a manterem seus elétrons ou a ganharem novos.

A Química Por Trás de Cada Atmosfera
O comportamento de uma atmosfera é definido por seu potencial de doar ou aceitar elétrons de um material. Este único princípio governa se um objeto irá enferrujar, queimar ou permanecer puro.
A Natureza Oxidante do Ar Comum
Nossa atmosfera normal é aproximadamente 21% oxigênio, um elemento altamente reativo. Isso torna nosso ambiente inerentemente oxidante.
Os átomos de oxigênio têm uma forte tendência a puxar elétrons de outros elementos. Este processo, conhecido como oxidação, é fundamental para reações como a ferrugem do ferro (formando óxido de ferro) ou a queima de madeira.
A Natureza Protetora de uma Atmosfera Redutora
Uma atmosfera redutora é um ambiente gasoso onde a oxidação é ativamente suprimida. Isso é conseguido de duas maneiras principais.
Primeiro, o oxigênio e outros agentes oxidantes são removidos ou significativamente diluídos. Segundo, gases que promovem a redução — o oposto químico da oxidação — são introduzidos. Gases redutores comuns incluem hidrogênio (H₂) e monóxido de carbono (CO).
Como Funcionam os Gases Redutores
Esses gases atuam como "removedores de oxigênio". Por exemplo, em altas temperaturas, qualquer oxigênio perdido reagirá preferencialmente com o hidrogênio para formar água (H₂O) ou com o monóxido de carbono para formar dióxido de carbono (CO₂).
Isso protege efetivamente um material de reagir com o próprio oxigênio. Neste ambiente, um átomo é mais propenso a ganhar um elétron (redução) do que a perdê-lo (oxidação).
Aplicações Práticas e Casos de Uso
A escolha entre uma atmosfera comum e uma redutora é crítica em muitos processos industriais e científicos onde a integridade do material é primordial.
Prevenindo a Formação de Carepa Durante o Tratamento Térmico
Quando metais são aquecidos a altas temperaturas em ar comum, sua superfície oxida rapidamente, formando uma camada quebradiça chamada "carepa".
O uso de uma atmosfera redutora durante o recozimento ou endurecimento impede a formação dessa carepa, resultando em um produto acabado mais limpo e de maior qualidade.
Fundição e Produção de Metais
O próprio processo de extração de metais como o ferro de seu minério natural (óxido de ferro) requer uma poderosa atmosfera redutora.
Em um alto-forno, a queima de coque cria um ambiente rico em monóxido de carbono. O monóxido de carbono remove os átomos de oxigênio do óxido de ferro, "reduzindo-o" de volta ao ferro puro e fundido.
Soldagem e Brasagem
A soldagem de alta qualidade requer a proteção do metal fundido contra o ar. Embora frequentemente feita com gases inertes como o argônio, uma mistura de gases contendo gases redutores como o hidrogênio pode ser usada.
Isso não apenas protege a poça de solda, mas também limpa ativamente a superfície, reduzindo quaisquer óxidos leves existentes, levando a uma ligação mais forte.
Compreendendo as Vantagens e Riscos
Embora poderosa, a criação e manutenção de uma atmosfera redutora envolve desafios e perigos significativos em comparação com o simples uso do ar ambiente.
Perigos de Inflamabilidade e Explosão
Os principais gases usados para criar atmosferas redutoras, hidrogênio e monóxido de carbono, são altamente inflamáveis e podem ser explosivos sob certas condições. Isso requer equipamentos especializados e protocolos de segurança rigorosos.
Toxicidade dos Agentes Redutores
O monóxido de carbono é um gás extremamente tóxico, incolor e inodoro. Qualquer processo que o utilize deve incorporar ventilação robusta e monitoramento contínuo do ar para proteger o pessoal.
Custo e Complexidade
Gerar uma mistura gasosa específica e manter sua pureza e pressão dentro de um forno ou câmara é muito mais complexo e caro do que usar uma atmosfera comum. O processo requer sistemas de controle precisos e um suprimento confiável de gases de alta pureza.
Fazendo a Escolha Certa para o Seu Objetivo
A atmosfera ideal é determinada inteiramente pelo resultado desejado para o seu material ou processo.
- Se seu foco principal é o aquecimento econômico sem preocupação com a oxidação da superfície: Uma atmosfera comum é a solução mais simples e barata.
- Se seu foco principal é preservar a pureza da superfície de um metal durante o tratamento térmico: Uma atmosfera redutora é necessária para prevenir a formação de carepa e manter a integridade do material.
- Se seu foco principal é transformar quimicamente um óxido de volta ao seu elemento puro (por exemplo, fundição): Uma forte atmosfera redutora não é apenas benéfica, é um requisito fundamental do processo.
Em última análise, dominar as condições atmosféricas lhe dá controle direto sobre o destino químico fundamental do seu material.
Tabela Resumo:
| Característica | Atmosfera Comum (Ar) | Atmosfera Redutora |
|---|---|---|
| Gás Primário | ~21% Oxigênio | Hidrogênio (H₂), Monóxido de Carbono (CO) |
| Efeito Químico | Promove Oxidação (Ferrugem) | Promove Redução (Previne Ferrugem) |
| Aplicação Chave | Aquecimento Geral | Tratamento Térmico de Metais, Fundição, Soldagem |
| Principal Risco | Formação de Carepa/Oxidação da Superfície | Inflamabilidade, Toxicidade (CO) |
Precisa de controle atmosférico preciso para seus processos de laboratório? A KINTEK é especializada em equipamentos e consumíveis de laboratório, fornecendo soluções para a criação de ambientes controlados para tratamento térmico, soldagem e síntese de materiais. Nossa experiência garante que seus materiais mantenham integridade e pureza. Entre em contato conosco hoje para discutir como podemos apoiar as necessidades específicas do seu laboratório!
Guia Visual
Produtos relacionados
- Célula de Fluxo de Redução de CO2 Personalizável para Pesquisa em NRR, ORR e CO2RR
- Forno de Hidrogênio com Atmosfera Inerte Controlada
- Forno com atmosfera controlada de correia de malha
As pessoas também perguntam
- Qual é a diferença entre uma célula voltaica e uma célula eletroquímica? Compreenda os Dois Tipos de Conversão de Energia
- Por que a célula eletroquímica deve ser continuamente purgada com nitrogênio? Garanta precisão em testes de corrosão de Ni-Cr
- Qual é a aplicação específica de uma célula eletroquímica na síntese de RPPO? Master Materiais de Alto Estado de Oxidação
- Por que as células de fluxo e os GDE são usados em testes de estabilidade CORR? Alcance Desempenho de Catalisador de Grau Industrial
- Por que uma célula de fluxo eletroquímica personalizada é usada para eCO2RR? Alcance Desempenho e Densidade de Cor de Grau Industrial


