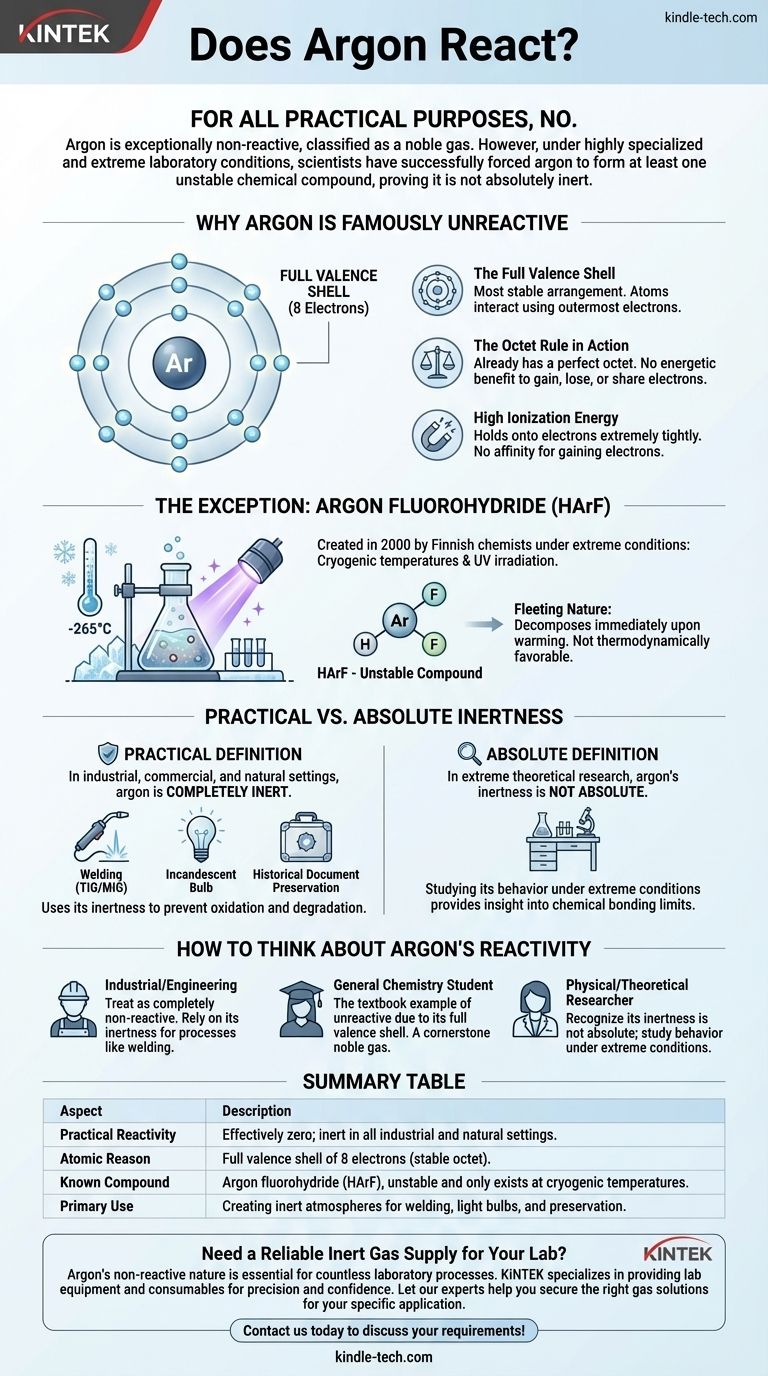
Para todos os efeitos práticos, não. O argônio é excepcionalmente não reativo, razão pela qual é classificado como um gás nobre. No entanto, sob condições de laboratório altamente especializadas e extremas, os cientistas conseguiram forçar o argônio a formar pelo menos um composto químico instável, provando que não é absolutamente inerte.
A principal conclusão é que a "reatividade" de um elemento não é uma questão simples de sim ou não. Embora a configuração perfeita da camada eletrônica do argônio o torne inerte em qualquer contexto natural ou industrial, sua não reatividade pode ser superada com energia suficiente sob condições criogênicas, revelando as sutis complexidades da ligação química.

Por que o Argônio é Famoso por Ser "Não Reativo"
Para entender por que o argônio resiste tão fortemente à formação de ligações químicas, devemos olhar para sua estrutura atômica. Sua reputação de ser inerte não é arbitrária; é um resultado direto de sua configuração eletrônica.
A Camada de Valência Completa
Os átomos interagem e formam ligações usando seus elétrons mais externos, conhecidos como elétrons de valência.
O argônio possui oito elétrons de valência, o que preenche completamente sua camada eletrônica externa. Esta é a configuração mais estável que um átomo pode ter.
A "Regra do Octeto" em Ação
A "regra do octeto" é um princípio fundamental na química que afirma que os átomos tendem a ganhar, perder ou compartilhar elétrons para atingir uma camada externa completa de oito elétrons.
Como o argônio já possui este octeto perfeito, não há benefício energético para ele ganhar, perder ou compartilhar elétrons com outros átomos. Ele já está em seu estado ideal de baixa energia.
Alta Energia de Ionização
A energia de ionização é a energia necessária para remover um elétron de um átomo. O argônio possui uma energia de ionização muito alta, o que significa que ele retém seus elétrons de forma extremamente forte.
Da mesma forma, ele não tem afinidade para ganhar elétrons. Simplesmente não há "motivo" químico para o argônio se envolver em uma reação em circunstâncias normais.
A Exceção Que Prova a Regra
Por décadas, acreditou-se que o argônio era completamente inerte. Isso mudou no ano 2000, quando uma equipe de químicos finlandeses criou o primeiro composto verdadeiro de argônio conhecido.
Forçando uma Reação Sob Condições Extremas
O composto, fluoridreto de argônio (HArF), não foi criado em um béquer de laboratório típico.
Os cientistas tiveram que congelar uma mistura de argônio e fluoreto de hidrogênio em uma superfície a temperaturas próximas do zero absoluto (cerca de -265°C ou -445°F) e, em seguida, irradiá-la com luz ultravioleta potente. Essa entrada de energia extrema foi suficiente para forçar temporariamente o relutante átomo de argônio a formar uma ligação.
A Natureza Fugaz dos Compostos de Argônio
O composto HArF resultante é incrivelmente instável. Ele só existe nessas temperaturas criogênicas.
Se for aquecido mesmo que ligeiramente, as ligações fracas se rompem, e ele se decompõe imediatamente de volta em argônio e fluoreto de hidrogênio separados. Isso destaca que o composto não é termodinamicamente favorável e existe apenas porque está "preso" pelo frio extremo.
Inércia Prática vs. Inércia Absoluta
Essa descoberta nos força a distinguir entre dois conceitos: o que é verdadeiro em um sentido prático e o que é verdadeiro em um sentido absoluto e teórico.
A Definição Prática de Inerte
Em qualquer ambiente industrial, comercial ou natural, o argônio é completamente inerte. Ele não reage com ar, água, metais ou qualquer outra substância com a qual entre em contato.
É essa inércia prática que o torna tão valioso.
Por Que Isso Importa Para as Aplicações
A não reatividade do argônio é uma característica, não uma limitação. Na soldagem (TIG/MIG), ele cria um "escudo" inerte ao redor do metal fundido, impedindo que ele oxide ou reaja com gases no ar, o que garante uma solda limpa e forte.
Em lâmpadas incandescentes, uma atmosfera de argônio impede que o filamento de tungstênio quente queime. Na preservação de documentos históricos, ele fornece um ambiente livre de oxigênio para impedir a degradação.
Como Pensar Sobre a Reatividade do Argônio
Seu contexto determina como você deve ver o comportamento químico do argônio. Compreender essa distinção é fundamental para aplicar os princípios químicos corretamente.
- Se você trabalha em um ambiente industrial ou de engenharia: Trate o argônio como um gás completamente não reativo. Sua inércia é sua propriedade mais valiosa e pode ser utilizada em processos como soldagem e fabricação.
- Se você é um estudante de química geral: Entenda que o argônio é o exemplo clássico de um elemento não reativo devido à sua camada de valência completa, tornando-o um pilar do grupo dos gases nobres.
- Se você é um pesquisador em química física ou teórica: Reconheça que a inércia do argônio não é absoluta, e o estudo de seu comportamento sob condições extremas fornece informações valiosas sobre os limites da ligação química.
Em última análise, a extrema relutância do argônio em reagir é uma propriedade fundamental que o torna cientificamente interessante e imensamente útil no mundo real.
Tabela Resumo:
| Aspecto | Descrição |
|---|---|
| Reatividade Prática | Efetivamente zero; inerte em todos os ambientes industriais e naturais. |
| Razão Atômica | Camada de valência completa de 8 elétrons (octeto estável). |
| Composto Conhecido | Fluoridreto de argônio (HArF), instável e existe apenas em temperaturas criogênicas. |
| Uso Principal | Criação de atmosferas inertes para soldagem, lâmpadas e preservação. |
Precisa de um Fornecimento Confiável de Gás Inerte para o Seu Laboratório?
A natureza não reativa do argônio é essencial para inúmeros processos laboratoriais, desde a criação de atmosferas controladas até o manuseio de materiais sensíveis. Garantir um suprimento consistente e de alta pureza é fundamental para seus resultados.
A KINTEK é especializada no fornecimento de equipamentos e consumíveis de laboratório de que você precisa para operar com precisão e confiança. Deixe nossos especialistas ajudá-lo a garantir as soluções de gás certas para sua aplicação específica.
Entre em contato conosco hoje mesmo através do nosso formulário para discutir suas necessidades!
Guia Visual