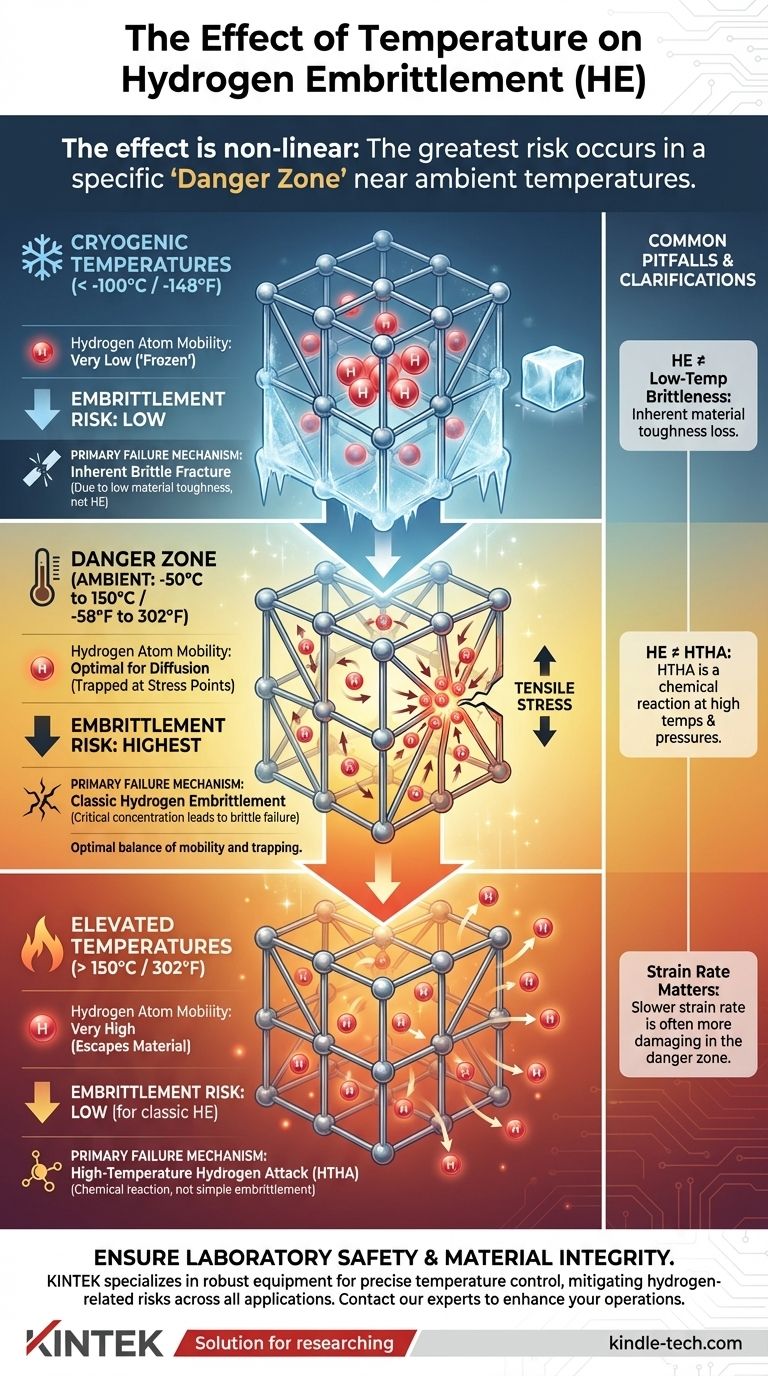
Em suma, o efeito da temperatura na fragilização por hidrogênio não é linear. O fenômeno é mais severo em uma faixa específica em torno da temperatura ambiente. Tanto temperaturas muito baixas (criogênicas) quanto elevadas reduzem significativamente o risco de fragilização clássica por hidrogênio, mas por razões inteiramente diferentes relacionadas à mobilidade dos átomos de hidrogênio.
O maior risco de falha por fragilização por hidrogênio ocorre perto das temperaturas ambientes, de aproximadamente -50°C a 150°C (-58°F a 302°F). Esta janela de temperatura cria um equilíbrio perigoso onde os átomos de hidrogênio são móveis o suficiente para encontrar pontos de tensão, mas não tão energéticos a ponto de escapar do material.

A Mecânica Subjacente: Mobilidade do Hidrogênio
Para entender o papel da temperatura, devemos primeiro reconhecer que a fragilização por hidrogênio requer três condições: um material suscetível (como aço de alta resistência), tensão de tração aplicada e uma fonte de hidrogênio atômico. O papel principal da temperatura é governar o comportamento desses átomos de hidrogênio dentro da rede cristalina do metal.
H3: A "Zona de Perigo" (Temperaturas Próximas ao Ambiente)
Esta faixa representa o maior risco porque oferece as condições ideais para a fragilização.
Os átomos de hidrogênio têm energia térmica suficiente para difundir, ou mover-se, através do metal. Essa mobilidade permite que eles migrem e se acumulem em áreas de alta tensão, como a ponta de uma microfissura.
Simultaneamente, a temperatura não é alta o suficiente para que o hidrogênio se difunda facilmente para fora do material. Essa combinação de mobilidade suficiente e aprisionamento eficaz leva a uma concentração crítica de hidrogênio em pontos de tensão, reduzindo severamente a ductilidade do material e levando a falhas súbitas e frágeis.
H3: Baixas Temperaturas (Condições Criogênicas)
À medida que a temperatura cai significativamente (por exemplo, abaixo de -100°C / -148°F), o risco de fragilização clássica por hidrogênio diminui.
Nessas temperaturas criogênicas, a taxa de difusão dos átomos de hidrogênio torna-se extremamente lenta. Os átomos ficam essencialmente "congelados" no lugar dentro da rede metálica.
Como eles não têm a mobilidade para viajar para áreas de alta tensão de tração, eles não podem se acumular nas concentrações críticas necessárias para causar a fragilização.
H3: Temperaturas Elevadas
Em temperaturas mais altas (por exemplo, acima de 150°C / 302°F), o risco de fragilização clássica por hidrogênio também diminui, mas pela razão oposta.
A taxa de difusão do hidrogênio torna-se muito alta. Essa mobilidade extrema significa que os átomos de hidrogênio podem facilmente difundir-se para fora do material para a atmosfera, evitando acúmulos internos perigosos.
Além disso, nessas temperaturas, o próprio metal torna-se mais dúctil e sua resistência ao escoamento diminui, tornando-o inerentemente menos propenso à fratura frágil.
Armadilhas Comuns e Esclarecimentos
Uma compreensão clara do efeito da temperatura requer a diferenciação da fragilização por hidrogênio de outros mecanismos de falha dependentes da temperatura.
H3: Não Confunda FE com Fragilidade a Baixas Temperaturas
Embora o risco de FE seja baixo em temperaturas criogênicas, o risco de um modo de falha diferente — fratura frágil — é muito alto para muitos aços. Isso se deve à perda intrínseca de tenacidade no próprio material em baixas temperaturas e é um fenômeno separado.
H3: Distinga FE de Ataque por Hidrogênio a Altas Temperaturas (HTHA)
Em temperaturas muito altas (tipicamente acima de 200°C / 400°F) e em ambientes de gás hidrogênio de alta pressão, um mecanismo diferente chamado Ataque por Hidrogênio a Altas Temperaturas (HTHA) pode ocorrer.
Este não é um processo simples de fragilização, mas uma reação química. O hidrogênio reage com os carbonetos no aço para formar gás metano, levando a rachaduras internas, bolhas e uma perda permanente de resistência. O HTHA é uma forma fundamentalmente diferente e irreversível de degradação do material.
H3: Considere o Impacto da Taxa de Deformação
O processo de fragilização é dependente do tempo. Na "zona de perigo", uma taxa de deformação mais lenta é frequentemente mais prejudicial porque dá aos átomos de hidrogênio mais tempo para difundir-se até a ponta de uma trinca em propagação, exacerbando o problema.
Fazendo a Escolha Certa para Sua Aplicação
Sua abordagem para mitigar falhas relacionadas ao hidrogênio deve ser adaptada à faixa de temperatura operacional específica do seu componente.
- Se o seu foco principal é o serviço criogênico (abaixo de -100°C): Sua principal preocupação é a tenacidade intrínseca do material, não a fragilização clássica por hidrogênio. Selecione materiais com excelentes valores de impacto Charpy V-notch na sua temperatura mínima de projeto.
- Se o seu componente opera perto de temperaturas ambientes (-50°C a 150°C): Você está na zona de maior risco. Priorize a seleção de materiais menos suscetíveis, controlando rigorosamente todas as potenciais fontes de hidrogênio (por exemplo, processos de fabricação como revestimento, soldagem ou corrosão em serviço) e gerenciando cuidadosamente as tensões de tração.
- Se você está operando em temperaturas elevadas (acima de 150°C): O risco de fragilização clássica é menor, mas você deve mudar sua análise para o risco separado e severo de Ataque por Hidrogênio a Altas Temperaturas (HTHA), especialmente para aços carbono e de baixa liga em serviço de hidrogênio.
Em última análise, a temperatura é a variável crítica que dita se o hidrogênio dentro de um material é um passageiro benigno ou um catalisador para falhas catastróficas.
Tabela Resumo:
| Faixa de Temperatura | Mobilidade do Átomo de Hidrogênio | Risco de Fragilização | Mecanismo Principal de Falha |
|---|---|---|---|
| Criogênica (< -100°C / -148°F) | Muito Baixa ("Congelada") | Baixo | Fratura Frágil Inerente (Tenacidade do Material) |
| Zona de Perigo (-50°C a 150°C / -58°F a 302°F) | Ótima para Difusão | Mais Alta | Fragilização Clássica por Hidrogênio |
| Elevada (> 150°C / 302°F) | Muito Alta (Escapa do Material) | Baixo (para FE) | Ataque por Hidrogênio a Altas Temperaturas (HTHA) |
Garanta que os materiais e equipamentos do seu laboratório estejam seguros contra falhas relacionadas ao hidrogênio. A KINTEK é especializada no fornecimento de equipamentos robustos de laboratório e consumíveis projetados para controle preciso de temperatura e integridade do material. Seja você trabalhando com aplicações criogênicas, condições ambientais ou processos de alta temperatura, nossas soluções ajudam a mitigar os riscos de fragilização por hidrogênio e outros mecanismos de falha. Entre em contato com nossos especialistas hoje para discutir como podemos apoiar as necessidades específicas do seu laboratório e aumentar a segurança e a confiabilidade de suas operações.
Guia Visual