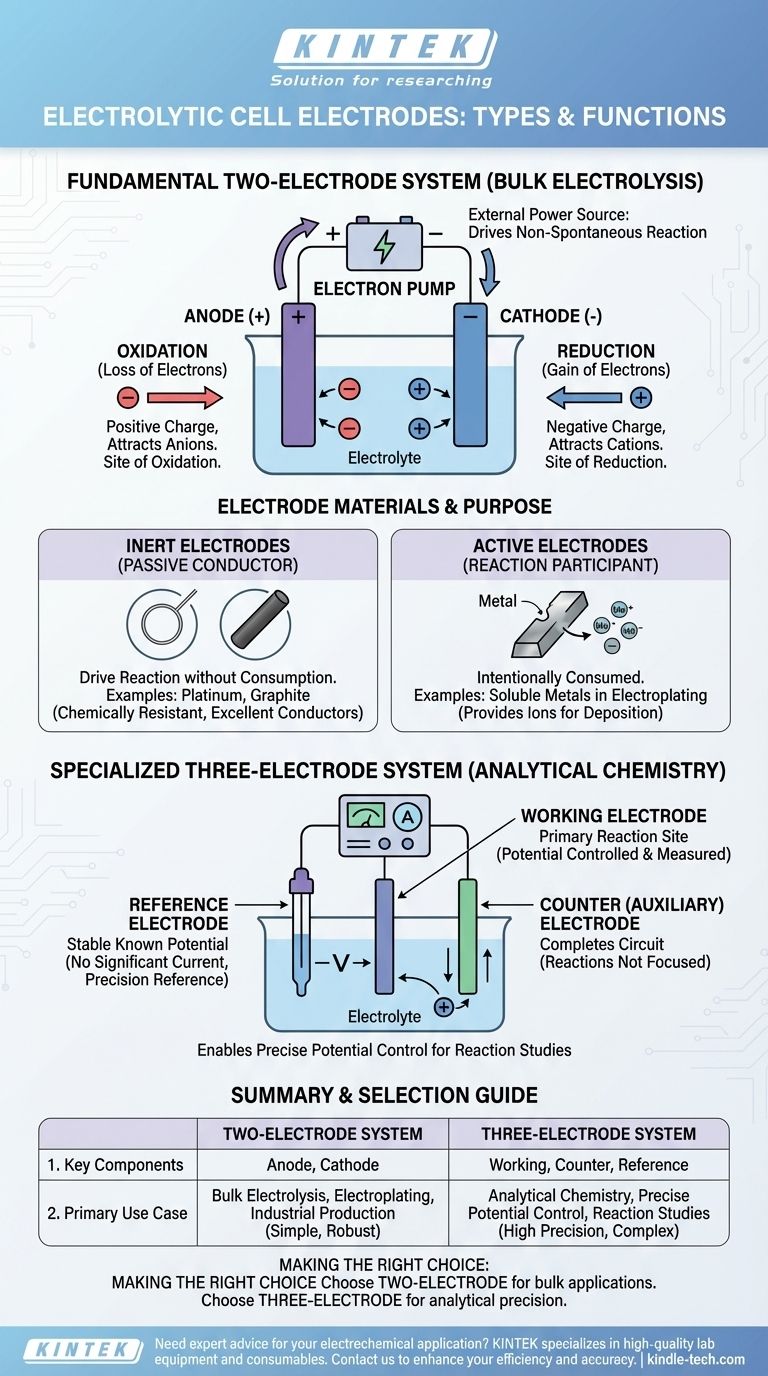
Em sua essência, uma célula eletrolítica usa dois eletrodos principais: um ânodo carregado positivamente onde ocorre a oxidação e um cátodo carregado negativamente onde ocorre a redução. Para trabalhos analíticos mais precisos, utiliza-se um sistema de três eletrodos, composto por um eletrodo de trabalho, um eletrodo auxiliar e um eletrodo de referência.
O tipo e o número de eletrodos usados em uma célula eletrolítica são determinados pelo seu propósito. Uma configuração simples de dois eletrodos (ânodo e cátodo) é suficiente para impulsionar uma reação química, enquanto um sistema de três eletrodos é necessário para medi-la e controlá-la com precisão.

O Sistema Fundamental de Dois Eletrodos
A maioria das células eletrolíticas, desde demonstrações em sala de aula até a produção em escala industrial, é construída com base em dois eletrodos. Este sistema utiliza uma fonte de energia externa para forçar a ocorrência de uma reação química não espontânea.
O Ânodo: Local da Oxidação
O ânodo é o eletrodo conectado ao terminal positivo da fonte de energia. Devido à sua carga positiva, ele atrai íons carregados negativamente (ânions) da solução eletrólita. Na superfície do ânodo, esses íons perdem elétrons em um processo chamado oxidação.
O Cátodo: Local da Redução
Inversamente, o cátodo é conectado ao terminal negativo da fonte de alimentação. Sua carga negativa atrai íons carregados positivamente (cátions). Na superfície do cátodo, esses íons ganham elétrons em um processo conhecido como redução.
O Papel da Fonte de Energia Externa
Ao contrário de uma bateria (célula galvânica) que gera tensão, uma célula eletrolítica a consome. A fonte de energia atua como uma "bomba de elétrons", retirando elétrons do ânodo e empurrando-os para o cátodo, impondo assim a carga e impulsionando todo o processo.
Materiais dos Eletrodos e Seu Propósito
O material de que um eletrodo é feito é fundamental para a função da célula. A escolha depende se o eletrodo deve ser um participante ativo ou um observador passivo na reação.
Eletrodos Inertes: O Condutor Passivo
Em muitas aplicações, o objetivo é impulsionar uma reação dentro do eletrólito sem que o próprio eletrodo seja consumido. Nesses casos, são usados eletrodos inertes. Materiais como platina e grafite (uma forma de carbono) são escolhas comuns porque são excelentes condutores elétricos, mas quimicamente resistentes e improváveis de reagir.
Eletrodos Ativos: O Participante da Reação
Em alguns processos, como galvanoplastia ou refino, o ânodo é intencionalmente projetado para ser consumido. Um eletrodo ativo é feito de um material que se oxida e se dissolve no eletrólito, fornecendo os íons metálicos que serão posteriormente depositados no cátodo.
O Sistema Especializado de Três Eletrodos
Para a química analítica, onde o objetivo é estudar uma reação em vez de realizar eletrólise em massa, é necessário um sistema de três eletrodos mais sofisticado. Esta configuração permite um controle extremamente preciso do potencial do eletrodo.
O Eletrodo de Trabalho
Este é o eletrodo principal onde ocorre a reação de interesse. Seu potencial elétrico é a variável que está sendo cuidadosamente controlada e medida.
O Eletrodo Auxiliar (ou Contra)
A única finalidade do eletrodo auxiliar é completar o circuito elétrico. A corrente flui entre o eletrodo de trabalho e o eletrodo auxiliar, mas as reações que ocorrem no eletrodo auxiliar não são o foco do experimento.
O Eletrodo de Referência
Esta é a chave para a precisão do sistema. Um eletrodo de referência fornece um potencial elétrico estável e conhecido. Nenhuma corrente significativa flui através dele, de modo que seu potencial permanece constante. Ao medir o potencial do eletrodo de trabalho em relação a esta referência estável, um pesquisador pode conhecer e controlar sua voltagem com alta precisão.
Compreendendo as Compensações
A escolha de um sistema envolve equilibrar a simplicidade com a necessidade de controle.
O Sistema de Dois Eletrodos: Simplicidade para Produção
Esta configuração é simples, robusta e ideal para aplicações em larga escala, como a produção de gás cloro ou alumínio. Sua limitação é a falta de controle preciso do potencial, pois a tensão aplicada é dividida de forma imprevisível entre os dois eletrodos e o eletrólito.
O Sistema de Três Eletrodos: Precisão para Análise
Este sistema oferece controle requintado, o que é essencial para estudar mecanismos de reação e realizar análises eletroquímicas sensíveis. No entanto, é mais complexo e geralmente usado para trabalhos de laboratório de baixa corrente, não para produção industrial.
Fazendo a Escolha Certa para o Seu Objetivo
Seu objetivo dita a configuração de eletrodo necessária.
- Se o seu foco principal for eletrólise em massa ou uma demonstração simples (por exemplo, separação de água, galvanoplastia): Um sistema de dois eletrodos (ânodo e cátodo) feito de materiais apropriados é a escolha correta e mais eficiente.
- Se o seu foco principal for medição analítica ou estudo de um mecanismo de reação: Um sistema de três eletrodos (trabalho, auxiliar, referência) é essencial para a precisão e o controle necessários.
Em última análise, entender a função de cada eletrodo permite que você selecione as ferramentas certas para a tarefa química em questão.
Tabela Resumo:
| Sistema de Eletrodos | Componentes Chave | Caso de Uso Principal |
|---|---|---|
| Dois Eletrodos | Ânodo (Oxidação), Cátodo (Redução) | Eletrólise em Massa, Galvanoplastia, Produção Industrial |
| Três Eletrodos | Eletrodos de Trabalho, Auxiliar, Referência | Química Analítica, Controle Preciso de Potencial, Estudos de Reação |
Precisa de aconselhamento especializado na seleção dos eletrodos corretos para sua aplicação eletroquímica? A KINTEK é especializada em equipamentos de laboratório e consumíveis de alta qualidade para todas as suas necessidades laboratoriais. Se você está se preparando para produção industrial ou trabalho analítico preciso, nossa equipe pode ajudá-lo a escolher o sistema ideal para aumentar sua eficiência e precisão. Entre em contato conosco hoje para discutir suas necessidades específicas!
Guia Visual
Produtos relacionados
- Célula Eletrolítica Tipo H Tripla Eletroquímica
- Célula de Gás de Eletrólise Eletroquímica Eletrolítica Célula de Reação de Fluxo Líquido
- Célula Eletrolítica de PTFE Célula Eletroquímica Resistente à Corrosão Selada e Não Selada
- Célula Eletroquímica Eletrolítica com Cinco Portas
- Célula Eletroquímica Eletrolítica Super Selada
As pessoas também perguntam
- O que deve ser observado durante um experimento com a célula eletrolítica tipo H? Monitoramento chave para resultados precisos
- O que é uma célula tipo H? Um Guia para Células Eletroquímicas Divididas para Experimentos Precisos
- Como o eletrólito deve ser preparado e adicionado à célula eletrolítica tipo H? Melhores práticas para pureza e segurança
- Quais características ópticas a célula eletrolítica tipo H possui? Janelas de quartzo de precisão para fotoeletroquímica
- Como deve ser armazenada a célula eletrolítica tipo H quando não estiver em uso? Guia Especializado de Armazenamento e Manutenção



















