A Ilusão da Simplicidade
No laboratório, muitas vezes nos fixamos na complexidade do eletrólito. Medimos concentrações até o micrograma. Obcecamos sobre gradientes de temperatura. Tratamos a solução química como uma receita delicada que requer o toque de um chef mestre.
No entanto, frequentemente negligenciamos o "encanamento" do experimento: os fios.
Conectar uma célula eletrolítica parece trivial. Fio vermelho aqui, fio preto ali. Parece ligar uma torradeira — realmente importa de que lado vai?
Na eletrólise, isso importa mais do que qualquer outra coisa.
A polaridade do eletrodo não é meramente um detalhe de conexão. É o centro de comando e controle do seu experimento. É a diferença entre criar uma obra-prima e dissolver seu equipamento.
A Bomba de Elétrons
Para entender a polaridade, você tem que parar de pensar na fonte de alimentação como uma bateria e começar a pensar nela como uma bomba.
Ao contrário de uma célula galvânica, onde a química cria eletricidade, uma célula eletrolítica usa eletricidade para forçar a química a acontecer contra sua vontade. A reação é não espontânea. Ela precisa de um impulso.
A fonte de alimentação fornece esse impulso, mas estritamente em uma direção:
- Ela puxa elétrons de um lado.
- Ela empurra elétrons para o outro.
Esse fluxo dita a identidade dos seus eletrodos. Os rótulos "Anodo" e "Catodo" não são locais geográficos no seu béquer; são papéis funcionais definidos inteiramente por esse fluxo.
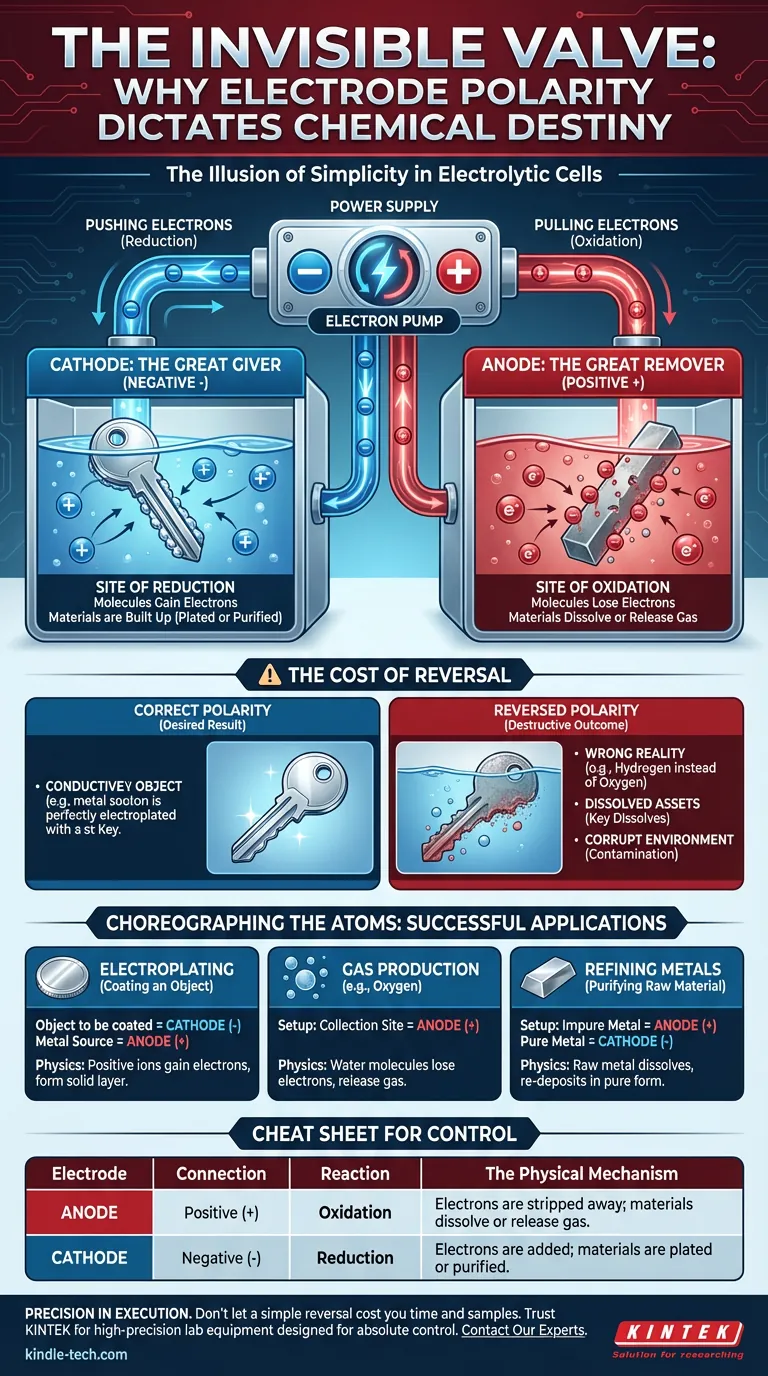
O Anodo: O Grande Removedor
Conectado ao terminal Positivo (+), o anodo é onde a fonte de alimentação arranca elétrons de espécies químicas.
Este é o local da Oxidação. Moléculas perto desta superfície perdem elétrons. Elas são despojadas.
O Catodo: O Grande Doador
Conectado ao terminal Negativo (-), o catodo é onde a fonte de alimentação força um excesso de elétrons para a superfície.
Este é o local da Redução. Moléculas perto desta superfície ganham elétrons. Elas são construídas.
O Custo da Inversão
O que acontece quando você inverte os fios?
Em muitas áreas da vida, uma conexão invertida apenas significa que o dispositivo não liga. Na eletrólise, as consequências são muito mais ativas — e frequentemente destrutivas.
Quando você inverte a polaridade, você não pausa a reação. Você inverte o universo do seu béquer.
1. Você fabrica a realidade errada
Se você pretendia gerar oxigênio, mas inverteu os terminais, pode gerar hidrogênio em vez disso. A lógica química é perfeitamente invertida. Você não está obtendo "nenhum resultado"; está obtendo o "anti-resultado".
2. Você dissolve seus bens
Imagine que você está galvanizando uma chave antiga com cobre. Você quer que os íons de cobre se depositem na chave.
Se você inverter a polaridade, a chave se torna o anodo (o local de oxidação). Em vez de receber uma camada brilhante de cobre, a própria chave começa a se dissolver na solução. Você não está preservando o objeto; você está ativamente destruindo-o.
3. Você corrompe o ambiente
Forçar a oxidação em um eletrodo não projetado para isso leva à corrosão rápida. Isso não apenas arruína o eletrodo; inunda seu eletrólito cuidadosamente preparado com contaminantes, invalidando todo o experimento.
Coreografando os Átomos
A eletrólise bem-sucedida exige que você seja um arquiteto do movimento atômico. Você deve decidir para onde os elétrons vão antes de apertar o interruptor.
Use esta lógica para atribuir sua polaridade:
-
O Objetivo: Galvanoplastia
- A Configuração: O objeto a ser revestido deve ser o Catodo (-).
- A Física: Você precisa que os íons metálicos positivos ganhem elétrons e se tornem metal sólido na superfície do objeto.
-
O Objetivo: Produção de Gás (por exemplo, Oxigênio)
- A Configuração: O local de coleta deve ser o Anodo (+).
- A Física: As moléculas de água devem perder elétrons (oxidar) para liberar gás oxigênio.
-
O Objetivo: Refino de Metais
- A Configuração: O metal impuro deve ser o Anodo (+).
- A Física: O metal bruto deve se dissolver (oxidar) na solução para que possa ser redepositado em forma pura em outro lugar.
O Resumo do Controle
Aqui está o guia rápido para controlar seu destino químico:
| Eletrodo | Conexão | Reação | O Mecanismo Físico |
|---|---|---|---|
| Anodo | Positivo (+) | Oxidação | Elétrons são arrancados; materiais se dissolvem ou liberam gás. |
| Catodo | Negativo (-) | Redução | Elétrons são adicionados; materiais são revestidos ou purificados. |
Precisão na Execução
Há um certo romance na eletrólise. Você está alcançando o mundo molecular e forçando os átomos a marchar na direção que você escolhe.
Mas esse controle depende da integridade da sua configuração. Mesmo o melhor entendimento teórico falha se o equipamento for não confiável ou as conexões forem ruins.
Na KINTEK, entendemos que a linha entre um avanço e um experimento falho é muitas vezes tão fina quanto uma conexão de fio. Somos especializados em equipamentos de laboratório e consumíveis de alta precisão projetados para lhe dar controle absoluto sobre seus processos eletroquímicos.
Se você está refinando metais preciosos ou realizando pesquisas sensíveis, nossas ferramentas garantem que, quando você comandar o fluxo de elétrons, eles irão exatamente para onde deveriam.
Não deixe que uma simples inversão lhe custe tempo e amostras. Entre em Contato com Nossos Especialistas
Guia Visual
Produtos relacionados
- Célula Eletrolítica de PTFE Célula Eletroquímica Resistente à Corrosão Selada e Não Selada
- Célula Eletroquímica Eletrolítica Super Selada
- Célula Eletroquímica Eletrolítica com Cinco Portas
- Célula Eletrolítica Tipo H Tripla Eletroquímica
- Célula de Gás de Eletrólise Eletroquímica Eletrolítica Célula de Reação de Fluxo Líquido
Artigos relacionados
- Conceção e normas de células electrolíticas
- A Arte da Resistência: Por Que Sua Célula Eletrolítica Precisa de Espaço para Respirar
- A Arquitetura da Certeza: Dominando o Controle em Células Eletrolíticas Multifuncionais
- A Geometria Silenciosa da Voltagem: Respeitando os Limites da Eletrólise
- O Parceiro Silencioso: Por que a Escolha do Material na Eletroquímica é uma Questão de Confiança




















