Para prevenir a oxidação, você deve usar um gás que desloque o oxigênio ambiente da área de trabalho. As escolhas mais comuns são gases inertes como Argônio (Ar) e Nitrogênio (N2), que criam um escudo não reativo. Em alguns processos industriais de alta temperatura, gases redutores como Hidrogênio (H2) ou misturas à base de hidrogênio também são usados para remover ativamente o oxigênio.
O princípio central não é apenas encontrar um único "gás anti-oxidação", mas controlar a atmosfera ao redor do seu material. Isso é alcançado ou protegendo passivamente a peça com um gás inerte ou limpando ativamente o ambiente com um gás redutor reativo.

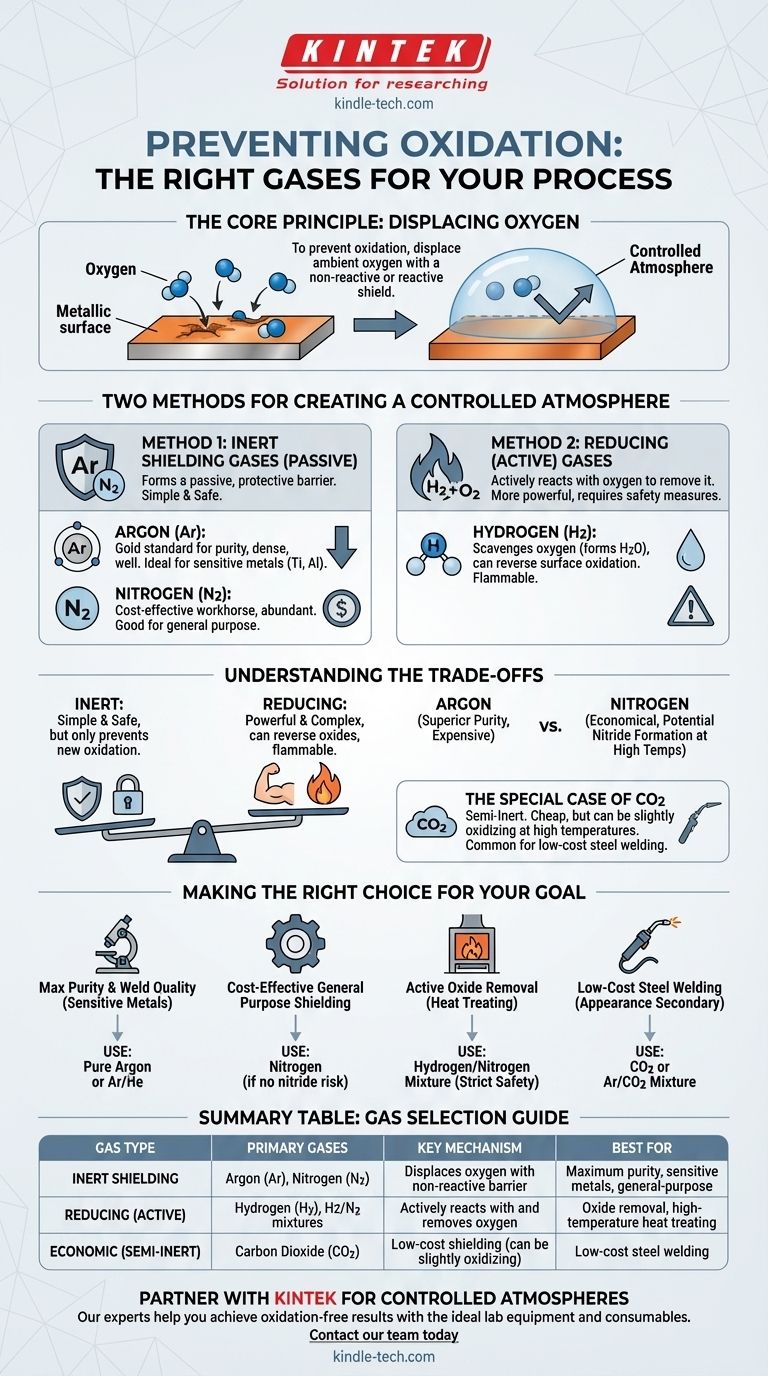
O Princípio Central: Deslocar o Oxigênio
A oxidação é uma reação química entre um material e o oxigênio, frequentemente acelerada pelo calor. Esse processo pode degradar as propriedades, a aparência e a integridade estrutural do material.
Para interromper essa reação, você deve remover um dos ingredientes chave: o oxigênio. Gases de blindagem ou purga realizam isso empurrando fisicamente o ar ambiente (que tem ~21% de oxigênio) para longe da superfície do material, criando uma atmosfera controlada.
Dois Métodos para Criar uma Atmosfera Controlada
Existem duas estratégias principais para prevenir a oxidação, cada uma usando diferentes tipos de gases que funcionam com princípios distintos.
Método 1: Gases de Blindagem Inertes
Gases inertes são quimicamente estáveis e não reagem facilmente com outros elementos, mesmo em altas temperaturas. Eles funcionam formando uma barreira protetora passiva.
Os dois gases de blindagem inertes mais comuns são:
- Argônio (Ar): Este é o padrão ouro para aplicações de alta pureza. Como é mais denso que o ar, ele cobre efetivamente uma área de trabalho, proporcionando excelente cobertura. É completamente inerte e não reage com nenhum material, tornando-o ideal para metais sensíveis como titânio, alumínio e aço inoxidável.
- Nitrogênio (N2): O Nitrogênio é o "cavalinho de batalha" de baixo custo. Ele compõe 78% do ar que respiramos e é muito mais barato de produzir do que o argônio. Funciona bem para muitas aplicações de uso geral.
Método 2: Gases Redutores (ou Ativos)
Gases redutores funcionam de forma mais ativa. Em vez de apenas bloquear o oxigênio, eles reagem com qualquer oxigênio presente (e até mesmo com óxidos existentes na superfície do material) para removê-lo.
O principal gás redutor é:
- Hidrogênio (H2): O hidrogênio é extremamente eficaz na eliminação de oxigênio, reagindo com ele para formar vapor de água (H₂O). Essa atmosfera "redutora" não só pode prevenir a oxidação, mas também pode limpar uma peça revertendo uma leve oxidação superficial. É frequentemente usado em misturas, como com nitrogênio na forma de amônia dissociada, para brasagem em forno e tratamento térmico.
Compreendendo as Compensações
A escolha do gás certo requer equilibrar desempenho, custo e segurança.
Inerte vs. Redutor
A principal compensação aqui é simplicidade versus poder. Os gases inertes são simples e seguros (não inflamáveis), mas apenas previnem a formação de nova oxidação.
Gases redutores como o hidrogênio são mais potentes e podem reverter óxidos existentes, mas são inflamáveis e exigem sistemas de manuseio e segurança mais complexos.
Argônio vs. Nitrogênio
O Argônio oferece proteção superior devido à sua densidade e inércia completa, mas é significativamente mais caro.
O Nitrogênio é altamente econômico, mas tem uma limitação chave: em temperaturas muito altas, pode reagir com certos metais (como titânio e alguns tipos de aço inoxidável) para formar nitretos indesejáveis, o que pode tornar o material quebradiço.
O Caso Especial do Dióxido de Carbono (CO2)
O dióxido de carbono é frequentemente usado em soldagem e às vezes é referido como um gás inerte, mas isso não é tecnicamente correto.
Nas altas temperaturas de um arco de solda, o CO2 pode se decompor em monóxido de carbono e oxigênio, levando a uma atmosfera mais reativa e ligeiramente oxidante em comparação com gases verdadeiramente inertes. É muito barato, mas oferece proteção de qualidade inferior à de uma mistura à base de argônio.
Fazendo a Escolha Certa para o Seu Objetivo
Os requisitos específicos da sua aplicação determinarão o melhor gás atmosférico.
- Se o seu foco principal for pureza máxima e qualidade de solda em metais sensíveis: Use Argônio puro ou uma mistura de Argônio/Hélio de alta pureza.
- Se o seu foco principal for blindagem de uso geral e econômica: O Nitrogênio é uma excelente escolha, desde que seu material e as temperaturas do processo não sejam suscetíveis à formação de nitretos.
- Se o seu foco principal for a remoção ativa de óxido durante o tratamento térmico em forno: Uma mistura de Hidrogênio/Nitrogênio é o padrão industrial, mas exige protocolos de segurança rigorosos.
- Se o seu foco principal for soldagem de aço de baixo custo onde a aparência é secundária: Uma mistura de CO2 ou Argônio/CO2 é uma escolha econômica comum.
Em última análise, selecionar o gás certo envolve alinhar as propriedades químicas da atmosfera com as necessidades do seu material e processo.
Tabela Resumo:
| Tipo de Gás | Gases Principais | Mecanismo Principal | Melhor Para |
|---|---|---|---|
| Blindagem Inerte | Argônio (Ar), Nitrogênio (N2) | Desloca o oxigênio com uma barreira não reativa | Pureza máxima, metais sensíveis, uso geral |
| Redutor (Ativo) | Hidrogênio (H2), misturas H2/N2 | Reage ativamente com e remove o oxigênio | Remoção de óxido, tratamento térmico de alta temperatura |
| Econômico (Semi-Inerte) | Dióxido de Carbono (CO2) | Blindagem de baixo custo (pode ser ligeiramente oxidante em altas temperaturas) | Soldagem de aço de baixo custo |
Precisa selecionar o gás perfeito para sua aplicação? A KINTEK é especializada em fornecer o equipamento de laboratório e consumíveis ideais para criar atmosferas controladas para seus materiais e processos específicos. Se você precisa de gases inertes de alta pureza para trabalhos sensíveis ou sistemas robustos para atmosferas redutoras ativas, nossos especialistas podem ajudá-lo a alcançar resultados livres de oxidação. Entre em contato com nossa equipe hoje para discutir suas necessidades e aprimorar as capacidades do seu laboratório!
Guia Visual