Um eletrodo de íon prata não aquoso é um eletrodo de referência altamente especializado, projetado especificamente para medições eletroquímicas em solventes orgânicos. Sua característica definidora é seu design configurável pelo usuário; ele é fornecido vazio, exigindo que o usuário prepare e adicione uma solução de preenchimento. Isso o torna uma ferramenta flexível, mas exigente, que fornece um potencial estável dentro de um único experimento, em vez de um potencial universal e absoluto como seus equivalentes aquosos.
O ponto crucial é que um eletrodo de íon prata não aquoso funciona como um eletrodo de quase-referência (QRE). Seu potencial não é fixo, mas depende da solução de preenchimento específica que você prepara. Para que os resultados sejam significativos e comparáveis, você deve calibrar seu potencial durante cada experimento usando um padrão interno como o ferroceno.

Características Principais do Design
A natureza física e química única deste eletrodo dita como ele deve ser manuseado e usado para garantir medições confiáveis.
Reservatório Preenchido pelo Usuário
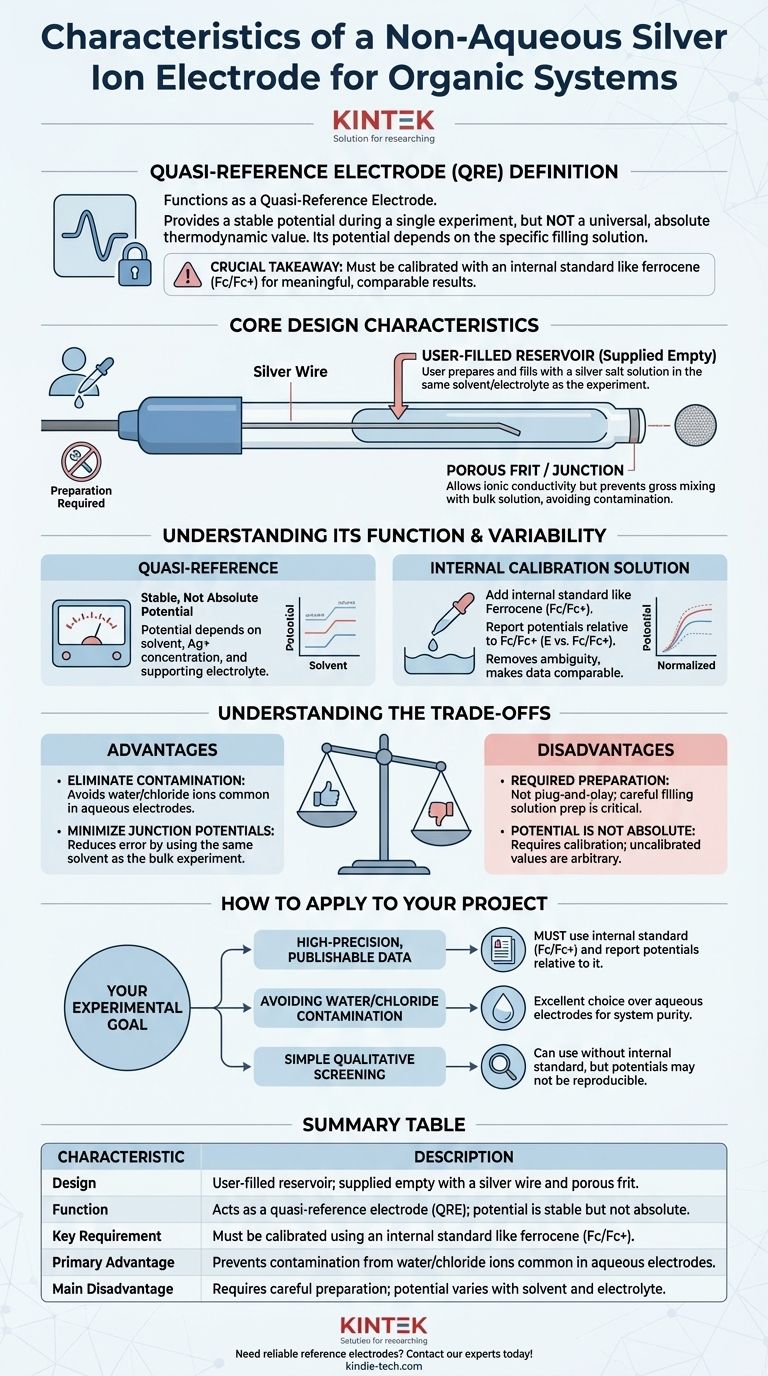
A característica mais notável é que o eletrodo é fornecido vazio. Ele consiste em um fio de prata alojado dentro de um corpo de vidro ou polímero que você deve preencher com uma solução apropriada. Esta é uma escolha de design deliberada, não uma medida de economia de custos.
O Papel da Solução de Preenchimento
Você cria o potencial de referência preparando uma solução de preenchimento, tipicamente uma concentração conhecida de um sal de prata (por exemplo, nitrato de prata, AgNO₃, ou triflato de prata, AgOTf) dissolvido no mesmo solvente e contendo o mesmo eletrólito de suporte do seu experimento principal. Esta preparação é o passo mais crítico para usar o eletrodo corretamente.
Isolamento da Solução Principal
A ponta do eletrodo apresenta uma frita porosa ou junção. Isso permite a condutividade iônica entre a solução de preenchimento interna e a solução principal em sua célula eletroquímica, o que é necessário para completar o circuito elétrico. No entanto, evita a mistura grosseira das duas soluções, o que contaminaria seu experimento e desestabilizaria o potencial de referência.
Compreendendo sua Função como Eletrodo de Quase-Referência (QRE)
O termo "eletrodo de quase-referência" descreve perfeitamente o comportamento de um eletrodo de íon prata preenchido pelo usuário em sistemas orgânicos.
O que é um QRE?
Um QRE fornece um potencial estável durante um único experimento contínuo. No entanto, este potencial não é baseado em um valor termodinâmico padronizado e universalmente acordado. É "quase" porque seu valor depende inteiramente da composição e concentração da solução de preenchimento que você preparou.
O Problema da Variabilidade do Potencial
O potencial do seu QRE Ag/Ag+ diferirá com base no solvente usado, na concentração do sal de prata e no eletrólito de suporte específico. Isso significa que um potencial de "+0,5 V" em um experimento não é diretamente comparável a "+0,5 V" em outro experimento se as condições ou a solução de preenchimento forem ligeiramente diferentes.
A Solução: Calibração Interna
Para obter dados significativos, reprodutíveis e publicáveis, você deve calibrar o QRE in situ. Isso é feito adicionando uma pequena quantidade de um padrão interno com um potencial redox bem conhecido à sua solução analítica.
Em eletroquímica não aquosa, o par ferroceno/ferrocênio (Fc/Fc+) é o padrão universalmente aceito. Após seu experimento, você simplesmente relata todos os potenciais medidos em relação ao potencial observado do par Fc/Fc+ (E vs. Fc/Fc+). Essa prática remove a ambiguidade do QRE e torna seus resultados comparáveis à pesquisa de qualquer outro laboratório.
Compreendendo as Compensações
O uso de um QRE não aquoso envolve um conjunto claro de vantagens e desvantagens que você deve ponderar para sua aplicação específica.
Vantagem: Eliminação da Contaminação
A principal razão para usar um eletrodo de referência não aquoso é evitar a contaminação de seu sistema orgânico sensível com água ou íons cloreto, que são inevitáveis ao usar eletrodos aquosos padrão como Ag/AgCl ou SCE.
Vantagem: Minimização dos Potenciais de Junção
Usar uma solução de preenchimento com o mesmo solvente do seu experimento principal reduz drasticamente o potencial de junção líquida. Este potencial grande, instável e desconhecido, que se forma na interface de dois solventes diferentes (por exemplo, água e acetonitrila), é uma grande fonte de erro ao usar eletrodos aquosos em meios orgânicos.
Desvantagem: Preparação Necessária
Este eletrodo não é "plug-and-play". Requer uma preparação cuidadosa da solução de preenchimento. Uma solução impropriamente preparada ou contaminada resultará em um potencial instável e flutuante que invalida toda a sua medição.
Desvantagem: O Potencial Não é Absoluto
Como discutido, o potencial é apenas estável, não absoluto. A falha em calibrar contra um padrão interno como o ferroceno significa que seus valores de potencial são arbitrários e não podem ser comparados ou reproduzidos de forma confiável.
Como Aplicar Isso ao Seu Projeto
O uso correto deste eletrodo depende inteiramente dos seus objetivos experimentais.
- Se seu foco principal são dados de alta precisão e publicáveis: Você deve usar um padrão interno como o ferroceno e relatar todos os potenciais em relação ao par redox Fc/Fc+.
- Se seu foco principal é evitar a contaminação por água/cloreto: Este eletrodo é uma excelente escolha em relação a qualquer alternativa aquosa, garantindo a pureza do seu sistema orgânico.
- Se seu foco principal é uma triagem qualitativa simples: Você pode usar o eletrodo sem um padrão interno, mas deve aceitar que os potenciais podem não ser perfeitamente reprodutíveis entre experimentos.
Devidamente preparado e calibrado, o eletrodo de íon prata não aquoso é uma ferramenta indispensável para análises eletroquímicas confiáveis em meios orgânicos.
Tabela Resumo:
| Característica | Descrição |
|---|---|
| Design | Reservatório preenchido pelo usuário; fornecido vazio com um fio de prata e frita porosa. |
| Função | Atua como um eletrodo de quase-referência (QRE); o potencial é estável, mas não absoluto. |
| Requisito Chave | Deve ser calibrado usando um padrão interno como o ferroceno (Fc/Fc+). |
| Vantagem Principal | Previne a contaminação por íons água/cloreto comuns em eletrodos aquosos. |
| Principal Desvantagem | Requer preparação cuidadosa; o potencial varia com o solvente e o eletrólito. |
Precisa de eletrodos de referência confiáveis para seu trabalho em eletroquímica orgânica? A KINTEK é especializada em equipamentos e consumíveis de laboratório de alta qualidade, incluindo eletrodos projetados para medições precisas e livres de contaminantes em sistemas não aquosos. Nossos produtos ajudam pesquisadores como você a obter resultados precisos e reprodutíveis. Entre em contato com nossos especialistas hoje para encontrar a solução perfeita para as necessidades do seu laboratório!
Guia Visual
Produtos relacionados
- Eletrodo de Referência Calomelano Cloreto de Prata Sulfato de Mercúrio para Uso Laboratorial
- Eletrodo de Referência de Sulfato de Cobre para Uso em Laboratório
- Eletrodo Auxiliar de Platina para Uso Laboratorial
- Eletrodo de Chapa de Platina para Aplicações Laboratoriais e Industriais
- Eletrodo de Disco de Ouro
As pessoas também perguntam
- Por que a seleção de um eletrodo de referência de alta qualidade é crucial na síntese eletroquímica? | KINTEK
- Qual é o propósito do eletrodo de referência? Obtenha Medições Eletroquímicas Estáveis e Precisas
- Qual é a manutenção recomendada para a solução de enchimento de um eletrodo de referência? Um Guia para Leituras Estáveis e Precisas
- Qual eletrodo é usado como referência de terra? Domine a Chave para Medições Eletroquímicas Precisas
- Qual eletrodo é usado como eletrodo de referência para medir potenciais de semi-células? Compreendendo o Padrão Universal








