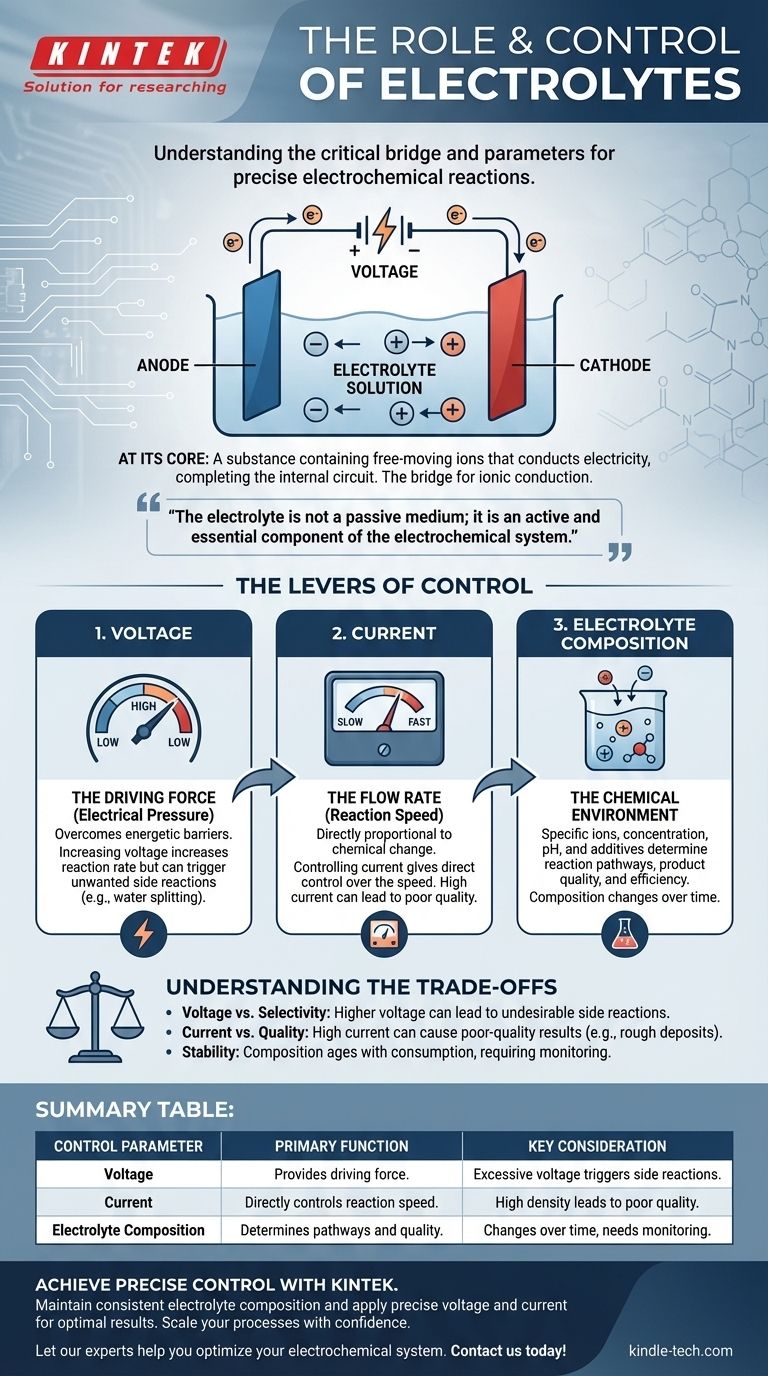
Em sua essência, um eletrólito é uma substância que contém íons de movimento livre que conduz eletricidade, completando o circuito dentro de uma célula eletroquímica. É a ponte crítica que permite que uma reação química seja impulsionada por uma fonte de energia externa. A própria reação é precisamente controlada ajustando três parâmetros chave: a tensão aplicada, a corrente resultante e a composição química do eletrólito.
O eletrólito não é um meio passivo; é um componente ativo e essencial do sistema eletroquímico. Entender como manipular as entradas elétricas e a química do eletrólito é a chave para transformar uma reação de um processo de força bruta em uma operação precisamente controlada.

O Papel Fundamental do Eletrólito
Para controlar um sistema, você deve primeiro entender seus componentes inegociáveis. Na eletroquímica, o eletrólito é o caminho interno que torna todo o processo possível.
O que é um Eletrólito?
Um eletrólito é tipicamente uma solução contendo sais, ácidos ou bases dissolvidos, que se dissociam em cátions carregados positivamente e ânions carregados negativamente. Embora frequentemente seja uma solução aquosa (à base de água), eles também podem ser baseados em solventes orgânicos ou até mesmo existir como sais fundidos em altas temperaturas.
A propriedade chave é a presença de íons móveis. Sem eles, o circuito interno é quebrado e nenhuma reação eletroquímica pode ocorrer.
A Ponte para a Condução Iônica
Uma célula eletroquímica possui dois circuitos. O circuito externo é a fiação através da qual os elétrons viajam de um eletrodo para o outro.
O circuito interno é o eletrólito. À medida que os elétrons chegam a um eletrodo (o cátodo) e partem do outro (o ânodo), os íons devem se mover através do eletrólito para equilibrar a carga. Os cátions se movem em direção ao cátodo e os ânions se movem em direção ao ânodo, completando o circuito elétrico.
Mais do que Apenas um Condutor
O eletrólito também participa ativamente da reação. Sua composição determina quais espécies químicas estão disponíveis para serem oxidadas ou reduzidas, quais serão os produtos da reação e quão rapidamente a reação pode prosseguir.
As Alavancas de Controle: Como Gerenciar a Reação
Controlar uma reação eletroquímica significa manipular a taxa e o resultado das mudanças químicas que ocorrem nos eletrodos. Isso é alcançado gerenciando as propriedades elétricas e químicas do sistema.
Controlando a Tensão (A Força Motriz)
A tensão pode ser pensada como a "pressão elétrica" que impulsiona a reação. Uma certa tensão mínima é necessária para superar a barreira energética de uma reação específica.
Aumentar a tensão geralmente aumenta a taxa de reação. No entanto, aplicar tensão excessiva é um instrumento grosseiro que pode desencadear reações secundárias indesejadas.
Controlando a Corrente (A Taxa de Fluxo)
A corrente é a medida de quantos elétrons estão fluindo através do circuito por unidade de tempo. De acordo com as leis de Faraday da eletrólise, a quantidade de mudança química é diretamente proporcional à quantidade de carga passada.
Portanto, controlar a corrente lhe dá controle direto sobre a velocidade da reação. Uma corrente constante (controle galvanostático) garante que a reação prossiga a uma taxa constante e previsível.
Ajustando a Composição do Eletrólito (O Ambiente Químico)
Este é o nível de controle mais sutil. Os íons específicos, sua concentração, o solvente e quaisquer aditivos mudam fundamentalmente o ambiente da reação.
Os fatores chave incluem concentração (que afeta a condutividade e a disponibilidade de íons), pH (que pode ditar quais reações são possíveis na água) e a presença de aditivos especializados que podem inibir a corrosão, abrilhantar um acabamento chapeado ou modificar o resultado de outra forma.
Entendendo as Compensações
O controle preciso requer a consciência das limitações e consequências de cada ajuste. Empurrar um parâmetro ao seu extremo muitas vezes compromete outro.
O Problema Tensão vs. Seletividade
Embora uma tensão mais alta aumente a taxa, ela também pode fornecer energia suficiente para iniciar reações indesejadas. Por exemplo, em uma solução aquosa, a tensão excessiva pode começar a dividir a água em hidrogênio e oxigênio, consumindo energia e reduzindo a eficiência do seu objetivo principal.
Densidade de Corrente e Qualidade
Buscar uma corrente muito alta (e, portanto, uma alta taxa de reação) pode levar a resultados de má qualidade. Na eletrodeposição, uma corrente muito alta pode fazer com que os íons se esgotem perto da superfície do eletrodo, resultando em um depósito áspero, poroso ou queimado. A qualidade geralmente requer paciência e uma densidade de corrente mais baixa.
Estabilidade e Vida Útil do Eletrólito
O eletrólito não é estático. Sua composição muda durante a reação à medida que os íons são consumidos e os contaminantes são introduzidos. Os solventes podem evaporar e os aditivos podem ser usados. Esse "envelhecimento" do eletrólito é uma fonte primária de inconsistência em processos industriais de longa duração e requer monitoramento e manutenção.
Fazendo a Escolha Certa para o Seu Objetivo
Sua estratégia de controle depende inteiramente do que você deseja alcançar. Use esses princípios para guiar sua abordagem.
- Se seu foco principal é maximizar a velocidade da reação: Use uma corrente mais alta e garanta que a concentração do eletrólito seja alta o suficiente para suportar essa taxa sem esgotamento significativo de íons perto dos eletrodos.
- Se seu foco principal é alcançar alta precisão ou qualidade: Use uma densidade de corrente mais baixa e cuidadosamente controlada ou aplique uma tensão específica (controle potenciostático) para garantir que a reação prossiga de forma suave e seletiva.
- Se seu foco principal é solucionar um processo inconsistente: Comece analisando o eletrólito. Sua composição, concentração e potencial contaminação são as fontes mais comuns de variabilidade do processo.
Dominar esses princípios transforma um processo eletroquímico de uma caixa preta em um sistema precisamente ajustável.
Tabela Resumo:
| Parâmetro de Controle | Função Primária | Consideração Chave |
|---|---|---|
| Tensão | Fornece a força motriz para a reação. | Tensão excessiva pode desencadear reações secundárias indesejadas. |
| Corrente | Controla diretamente a velocidade da reação. | Alta densidade de corrente pode levar a resultados de má qualidade. |
| Composição do Eletrólito | Determina os caminhos da reação e a qualidade do produto. | A composição muda ao longo do tempo, exigindo monitoramento. |
Pronto para alcançar controle preciso sobre seus processos eletroquímicos?
Na KINTEK, somos especializados em fornecer o equipamento de laboratório e os consumíveis de alta qualidade que você precisa para dominar suas reações. Seja você desenvolvendo novos materiais, realizando eletrodeposição ou conduzindo pesquisas, nossas soluções o ajudam a:
- Manter uma composição consistente do eletrólito para resultados confiáveis.
- Aplicar controle preciso de tensão e corrente para ótima seletividade e qualidade.
- Dimensionar seus processos da bancada de laboratório para a produção com confiança.
Deixe nossos especialistas ajudá-lo a otimizar seu sistema eletroquímico. Entre em contato conosco hoje para discutir sua aplicação e desafios específicos!
Guia Visual
Produtos relacionados
- Célula Eletrolítica Eletroquímica para Avaliação de Revestimentos
- Célula Eletroquímica Eletrolítica Super Selada
- Célula Eletroquímica Eletrolítica com Cinco Portas
- Célula de Gás de Eletrólise Eletroquímica Eletrolítica Célula de Reação de Fluxo Líquido
- Membrana de Troca de Prótons para Aplicações de Laboratório em Baterias
As pessoas também perguntam
- Qual é a diferença entre célula eletrolítica e eletrodo? Domine os Fundamentos dos Sistemas Eletroquímicos
- Para que tipo de sistema de eletrodos é projetada a célula eletrolítica de avaliação de revestimento? Desbloqueie a Análise Precisa de Revestimentos
- Por que a célula eletroquímica deve ser continuamente purgada com nitrogênio? Garanta precisão em testes de corrosão de Ni-Cr
- Qual é o procedimento para iniciar o experimento e o que deve ser observado? Um Guia Passo a Passo para Eletroquímica Confiável
- Qual é o procedimento correto de desligamento e desmontagem após um experimento? Garanta a Segurança e Proteja Seu Equipamento



















