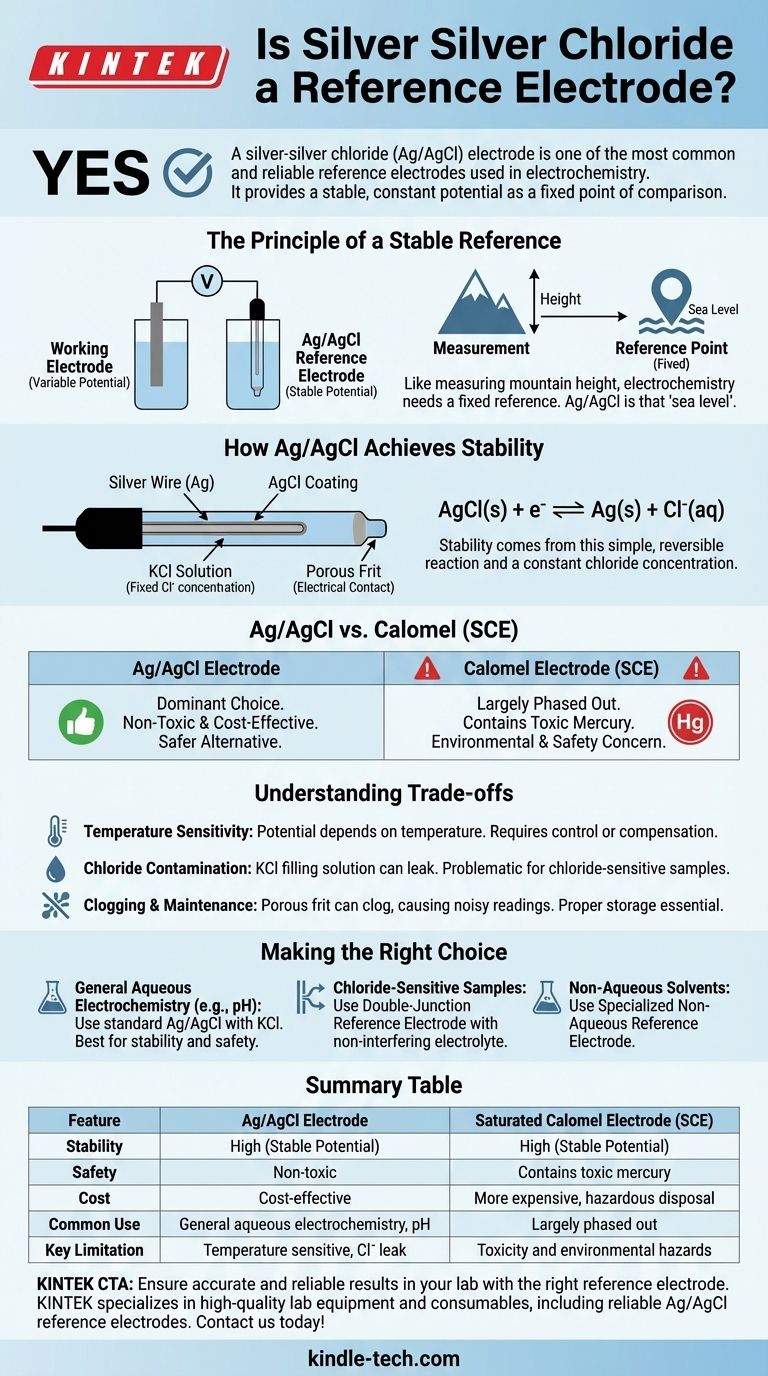
Sim, um eletrodo de prata-cloreto de prata (Ag/AgCl) é um dos eletrodos de referência mais comuns e confiáveis usados em eletroquímica. Ele fornece um potencial estável e constante que atua como um ponto fixo de comparação, permitindo medir com precisão o potencial de outro eletrodo (o eletrodo de trabalho) dentro de uma célula eletroquímica. Essa estabilidade o torna indispensável para aplicações que vão desde a medição de pH até a voltametria cíclica.
A função principal de um eletrodo de referência é fornecer uma linha de base de voltagem inalterável. O eletrodo de Ag/AgCl consegue isso através de um equilíbrio químico específico e estável, tornando-o um padrão confiável e econômico na eletroquímica moderna.

O Princípio de uma Referência Estável
Para entender por que o eletrodo de Ag/AgCl é tão eficaz, devemos primeiro entender o que torna uma boa referência. Uma medição eletroquímica é sempre uma comparação de potencial entre dois pontos.
O que é um Eletrodo de Referência?
Um eletrodo de referência é uma semicélula com um potencial de eletrodo conhecido e estável. Sua função é permanecer constante, independentemente das mudanças que ocorrem na outra metade da célula (o eletrodo de trabalho e a solução da amostra).
Pense nisso como medir a altura de uma montanha. Você precisa de um ponto de referência fixo, como o nível do mar, para obter uma medição significativa. Em eletroquímica, o eletrodo de referência é o nível do mar.
Como o Ag/AgCl Atinge Estabilidade
A estabilidade do eletrodo de Ag/AgCl vem de uma reação química simples e reversível. Consiste em um fio de prata revestido com uma fina camada de cloreto de prata (AgCl), tudo imerso em uma solução com uma concentração fixa de íons cloreto (Cl⁻), tipicamente cloreto de potássio (KCl).
O potencial é estabelecido pelo equilíbrio entre o metal prata sólido e seu sal:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
Como a concentração da solução de cloreto dentro do eletrodo é mantida constante, o potencial dessa semirreação permanece excepcionalmente estável.
Ag/AgCl vs. Outros Eletrodos de Referência
O eletrodo de Ag/AgCl não é a única opção, mas suas vantagens o tornaram uma escolha dominante sobre padrões mais antigos, como o Eletrodo de Calomelano Saturado (ECS).
A Ascensão do Ag/AgCl
A principal razão para a ampla adoção do Ag/AgCl é sua segurança e desempenho. É relativamente barato de produzir e, o mais importante, não tóxico.
O Declínio do Eletrodo de Calomelano (ECS)
O eletrodo de Calomelano, que usa uma pasta de mercúrio/cloreto mercuroso, já foi um padrão comum. No entanto, ele foi amplamente descontinuado em muitos laboratórios.
A principal razão é a toxicidade. O mercúrio é um material perigoso, tornando o uso, armazenamento e descarte de eletrodos de Calomelano uma preocupação ambiental e de segurança significativa.
Compreendendo as Compensações
Embora o eletrodo de Ag/AgCl seja uma excelente escolha para fins gerais, ele não está isento de limitações. Compreender essas compensações é crucial para medições precisas.
Sensibilidade à Temperatura
O potencial de um eletrodo de Ag/AgCl depende da temperatura. Para trabalhos de alta precisão, a temperatura da célula deve ser controlada e relatada, ou uma sonda de compensação de temperatura deve ser usada.
Contaminação por Cloreto
O eletrodo é preenchido com uma solução concentrada de KCl. Uma pequena quantidade dessa solução pode vazar da frita porosa na ponta do eletrodo para a amostra. Se seu experimento for sensível a íons cloreto, isso pode ser uma fonte de erro.
Obstrução e Manutenção
A frita porosa que permite o contato elétrico com a amostra pode ficar obstruída, levando a leituras de potencial ruidosas ou flutuantes. O armazenamento adequado (com a ponta imersa em sua solução de preenchimento) e a manutenção regular são essenciais para uma longa vida útil e resultados precisos.
Fazendo a Escolha Certa para Sua Aplicação
A seleção do eletrodo de referência e da solução de preenchimento corretos é crítica para o sucesso experimental. Sua escolha depende inteiramente da química de sua amostra.
- Se você estiver realizando eletroquímica aquosa geral (como a maioria das medições de pH ou íons): Um eletrodo de Ag/AgCl com uma solução de preenchimento de KCl padrão é quase sempre a melhor escolha devido à sua estabilidade e segurança.
- Se sua amostra reage ou é sensível a íons cloreto: Você deve usar um eletrodo de referência de "junção dupla", onde uma câmara externa com um eletrólito não interferente (como nitrato de potássio) isola o elemento interno de Ag/AgCl de sua amostra.
- Se você estiver trabalhando em solventes não aquosos: Você precisará de um eletrodo de referência não aquoso especializado, pois os eletrodos aquosos padrão não funcionarão corretamente e contaminarão seu solvente.
Em última análise, escolher o eletrodo de referência certo é garantir que ele permaneça um observador inerte e estável da reação química que você deseja estudar.
Tabela Resumo:
| Característica | Eletrodo Ag/AgCl | Eletrodo de Calomelano Saturado (ECS) |
|---|---|---|
| Estabilidade | Alta (potencial estável) | Alta (potencial estável) |
| Segurança | Não tóxico | Contém mercúrio tóxico |
| Custo | Custo-benefício | Mais caro, descarte perigoso |
| Uso Comum | Eletroquímica aquosa geral, medição de pH | Amplamente descontinuado devido a preocupações de segurança |
| Principal Limitação | Sensível à temperatura, potencial contaminação por cloreto | Toxicidade e riscos ambientais |
Garanta resultados precisos e confiáveis em seu laboratório com o eletrodo de referência certo. A KINTEK é especializada em equipamentos e consumíveis de laboratório de alta qualidade, incluindo eletrodos de referência Ag/AgCl confiáveis, adaptados para suas aplicações eletroquímicas. Nossos especialistas podem ajudá-lo a selecionar o eletrodo perfeito para manter a estabilidade e evitar a contaminação em seus experimentos. Entre em contato conosco hoje para aprimorar a precisão e segurança do seu laboratório!
Guia Visual
Produtos relacionados
- Eletrodo de Referência Calomelano Cloreto de Prata Sulfato de Mercúrio para Uso Laboratorial
- Eletrodo de Referência de Sulfato de Cobre para Uso em Laboratório
- Célula de Gás de Eletrólise Eletroquímica Eletrolítica Célula de Reação de Fluxo Líquido
- Eletrodo Eletroquímico de Carbono Vítreo
- Eletrodo Eletroquímico de Grafite em Disco, Haste e Chapa
As pessoas também perguntam
- Qual eletrodo é usado como referência de terra? Domine a Chave para Medições Eletroquímicas Precisas
- Como a seleção de eletrodos de referência, como Ag/AgCl ou Hg/HgO, se correlaciona com o pH do eletrólito em testes de reação de evolução de hidrogênio (HER)?
- Qual é a manutenção recomendada para a solução de enchimento de um eletrodo de referência? Um Guia para Leituras Estáveis e Precisas
- Qual é o propósito do eletrodo de referência? Obtenha Medições Eletroquímicas Estáveis e Precisas
- Qual é a função de um eletrodo de referência? Domine a precisão na reconstrução de reatores de três eletrodos











