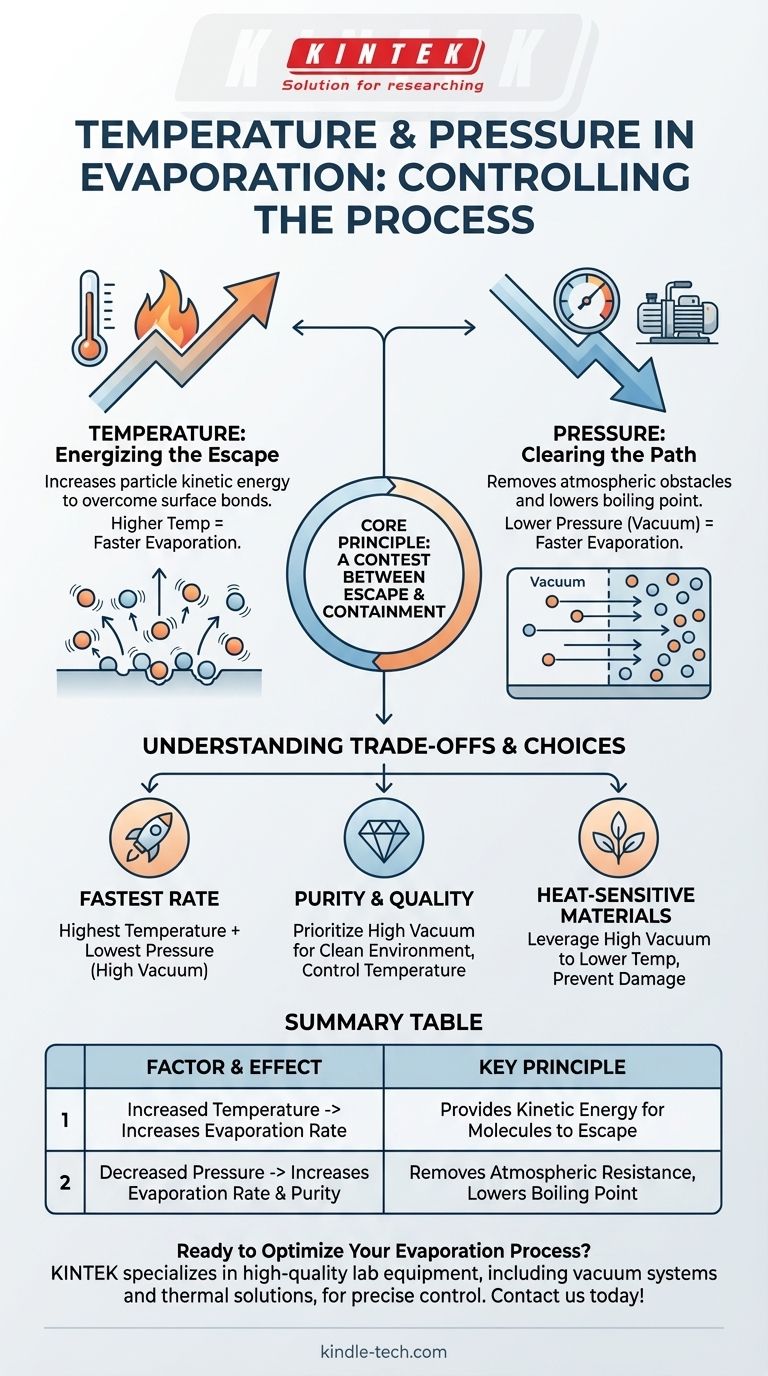
Em qualquer processo de evaporação, a temperatura e a pressão são as duas principais alavancas de controle. O aumento da temperatura fornece energia às moléculas para escapar de uma superfície, aumentando assim a taxa de evaporação. Por outro lado, a diminuição da pressão ambiente remove obstáculos atmosféricos, o que também aumenta significativamente a taxa de evaporação.
O princípio central é uma disputa entre escape e contenção. A temperatura dá às moléculas a energia para escapar, enquanto a pressão mais baixa remove as forças externas que as contêm, tornando todo o processo mais rápido e eficiente.

O Papel da Temperatura: Energizando o Escape
A temperatura é a forma mais direta de influenciar a rapidez com que um material evapora. A relação é baseada na energia de átomos ou moléculas individuais.
A Energia Cinética é Fundamental
A temperatura é fundamentalmente uma medida da energia cinética média (a energia do movimento) das partículas em uma substância.
Ao aquecer um material, você está aumentando a velocidade e a vibração de suas partículas constituintes.
Superando as Ligações Superficiais
Para uma partícula evaporar, ela deve ter energia suficiente para quebrar as ligações que a prendem à superfície do material.
Temperaturas mais altas significam que uma porcentagem maior de partículas possui essa "velocidade de escape" necessária, levando a uma taxa de evaporação geral mais alta.
Aplicação na Deposição de Materiais
Em processos como a deposição de filmes finos, o aquecimento do substrato alvo é crítico. Como mencionado, o aquecimento acima de 150 °C garante boa adesão.
Isso ocorre porque os átomos depositados chegam com energia térmica suficiente para se moverem ligeiramente na superfície, assentando-se em uma estrutura cristalina estável, uniforme e bem ligada.
O Papel da Pressão: Abrindo o Caminho
Enquanto a temperatura fornece o "impulso" para a evaporação, a pressão ambiente fornece o "contra-impulso". Gerenciar essa pressão externa é muitas vezes tão importante quanto.
Resistência Atmosférica
O ar ou gás acima de uma superfície exerce pressão, criando uma camada de partículas que um átomo em evaporação deve atravessar.
Na pressão atmosférica padrão, uma partícula em evaporação colidirá com bilhões de moléculas de ar, diminuindo seu progresso e até mesmo a derrubando de volta à superfície.
O Poder do Vácuo
Diminuir a pressão, ou criar um vácuo, remove essas partículas atmosféricas. Isso abre o caminho para os átomos em evaporação.
Em alto vácuo, um átomo pode viajar em linha reta de sua fonte para seu destino (como um substrato) com uma chance muito menor de colisão, aumentando dramaticamente a taxa de evaporação líquida.
Diminuindo o Ponto de Ebulição
Um efeito crítico da diminuição da pressão é que ela reduz o ponto de ebulição do material. A ebulição é simplesmente uma evaporação rápida que ocorre quando a pressão de vapor interna de um material é igual à pressão ambiente externa.
Ao criar um vácuo, você pode fazer com que os materiais evaporem ou fervam em temperaturas muito mais baixas do que seria possível em ar aberto. Isso é essencial para o processamento de materiais sensíveis ao calor.
Compreendendo as Compensações
Controlar a temperatura e a pressão permite resultados precisos, mas exige o equilíbrio de fatores concorrentes.
Pureza vs. Taxa
Em uma câmara de vácuo, o objetivo muitas vezes não é apenas uma alta taxa, mas alta pureza. Uma pressão mais baixa garante que menos moléculas de gás contaminantes (como oxigênio ou nitrogênio) estejam presentes para interferir ou serem incorporadas no filme final depositado.
Custos de Energia vs. Custos de Equipamento
Atingir altas temperaturas requer um consumo significativo de energia. Atingir um alto vácuo requer sistemas de bombeamento caros e complexos.
A escolha geralmente depende das propriedades do material. Pode ser mais eficiente usar um vácuo moderado e uma temperatura mais alta para um material robusto, ou um alto vácuo e uma temperatura mais baixa para um material delicado.
Fazendo a Escolha Certa para o Seu Objetivo
As configurações ideais para temperatura e pressão dependem inteiramente do que você está tentando alcançar com o processo de evaporação.
- Se o seu foco principal é a taxa de evaporação mais rápida possível: Use a temperatura mais alta que o material pode tolerar combinada com a menor pressão possível (maior vácuo).
- Se o seu foco principal é a pureza do material e a qualidade do filme: Priorize a obtenção de um alto vácuo para criar um ambiente limpo e, em seguida, aplique cuidadosamente a temperatura para controlar a taxa de deposição.
- Se o seu foco principal é o processamento de um material sensível ao calor: Aproveite um alto vácuo para diminuir significativamente a temperatura de evaporação, evitando assim danos térmicos à substância.
Em última análise, dominar a evaporação é entender como usar a temperatura e a pressão em conjunto para atingir seus objetivos específicos de material.
Tabela Resumo:
| Fator | Efeito na Evaporação | Princípio Chave |
|---|---|---|
| Aumento da Temperatura | Aumenta a taxa de evaporação | Fornece energia cinética para as moléculas escaparem da superfície |
| Diminuição da Pressão | Aumenta a taxa de evaporação e pureza | Remove a resistência atmosférica, diminui o ponto de ebulição |
Pronto para Otimizar Seu Processo de Evaporação?
Compreender a interação entre temperatura e pressão é crucial para alcançar resultados precisos em seu laboratório. Seja para maximizar a pureza, proteger materiais sensíveis ao calor ou aumentar as taxas de deposição, ter o equipamento certo é fundamental.
A KINTEK é especializada em equipamentos de laboratório de alta qualidade, incluindo sistemas de vácuo e soluções térmicas, projetados para oferecer controle preciso sobre seus processos. Nossos especialistas podem ajudá-lo a selecionar a configuração ideal para sua aplicação específica, garantindo eficiência, confiabilidade e resultados superiores.
Entre em contato conosco hoje para discutir suas necessidades e descobrir como a KINTEK pode aprimorar as capacidades do seu laboratório!
Guia Visual
Produtos relacionados
- Crisol e Barco de Evaporação de Cobre Livre de Oxigênio para Revestimento por Evaporação de Feixe de Elétrons
- Barco de Evaporação de Molibdênio, Tungstênio e Tântalo para Aplicações de Alta Temperatura
- Revestimento por Evaporação de Feixe de Elétrons Galvanoplastia Cadinho de Tungstênio Molibdênio para Evaporação
- Barco de Evaporação de Tungstênio-Molibdênio com Fundo Hemisférico
- Barco de Evaporação para Matéria Orgânica
As pessoas também perguntam
- Qual é a temperatura da evaporação por feixe de elétrons? Dominando o Processo Térmico de Duas Zonas para Filmes de Precisão
- O que é evaporação por feixe de elétrons? Obtenha Deposição de Filmes Finos de Alta Pureza para o Seu Laboratório
- Como é chamado o recipiente que contém o material de origem metálico na evaporação por feixe de elétrons? Garanta Pureza e Qualidade na Sua Deposição de Filmes Finos
- Para que serve a evaporação por feixe de elétrons? Revestimento de Precisão para Óptica, Aeroespacial e Eletrônica
- Como um evaporador de feixe de elétrons é resfriado durante a deposição? Gerenciamento Térmico Essencial para Processos Estáveis


















