Em um ambiente de laboratório, a remoção de um solvente por evaporação envolve a aplicação de energia, tipicamente como calor, e/ou a redução da pressão ambiente. Isso fornece às moléculas do solvente energia suficiente para escapar para a fase gasosa, deixando para trás os componentes menos voláteis da sua mistura, como o produto desejado. Este processo é gerenciado ativamente usando equipamentos específicos para controlar a velocidade e a temperatura.
O desafio central da remoção de solvente não é apenas a evaporação, mas a evaporação controlada. Seu objetivo é remover o solvente o mais rápido possível sem degradar ou perder a amostra que você está tentando isolar. O melhor método sempre depende das propriedades do solvente e da sensibilidade da amostra.

Os Princípios Centrais da Evaporação
Para escolher o método certo, você deve primeiro entender os quatro fatores que pode manipular para controlar a velocidade da evaporação. Esses princípios são a base de toda técnica.
O Papel da Temperatura
Aumentar a temperatura de um solvente aumenta diretamente a energia cinética de suas moléculas. Isso torna mais fácil para elas superarem as forças que as mantêm na fase líquida e escaparem como gás. Mais calor significa evaporação mais rápida.
O Papel da Pressão
Reduzir a pressão acima de um líquido diminui seu ponto de ebulição. Este é o princípio mais importante para manusear amostras sensíveis. Ao colocar uma amostra sob vácuo, você pode fazer o solvente ferver e evaporar em uma temperatura muito mais baixa e segura, protegendo seu composto da degradação térmica.
O Papel da Área de Superfície
A evaporação ocorre apenas na superfície do líquido. Ao aumentar a área de superfície, você expõe mais moléculas de solvente à fase gasosa, acelerando drasticamente o processo. É por isso que uma poça evapora mais rápido do que a mesma quantidade de água em um copo fundo.
O Papel do Fluxo de Gás
Quando um solvente evapora, ele cria uma camada de vapor logo acima da superfície do líquido, o que pode levar à reconensação. Ao soprar um fluxo constante de um gás inerte (como nitrogênio) sobre a superfície, você empurra constantemente esse vapor para longe, incentivando mais do líquido a evaporar para restaurar o equilíbrio.
Métodos Comuns de Evaporação em Laboratório
Esses princípios são aplicados usando vários equipamentos de laboratório padrão, cada um adequado para diferentes escalas e tipos de amostras.
Evaporação Simples em Capela de Exaustão
Este é o método mais básico. A amostra é colocada em um recipiente largo e raso (como um prato de evaporação ou vidro de relógio) dentro de uma capela de exaustão. O fluxo de ar da capela fornece um fluxo de gás suave para carregar os vapores.
Este método é adequado apenas para volumes muito pequenos de solventes não tóxicos e altamente voláteis e para amostras que não são sensíveis ao ar ou à exposição prolongada.
Aquecimento em Placa de Aquecimento
Uma maneira simples de acelerar a evaporação é aquecer suavemente a amostra em uma placa de aquecimento em uma capela de exaustão. Isso aplica diretamente o princípio de aumento da temperatura.
Embora rápido, este método oferece controle de temperatura deficiente e cria um alto risco de superaquecimento ou "ebulição violenta" (ebulição violenta), o que pode levar à perda e degradação da amostra.
Evaporação por Sopro de Nitrogênio
Também conhecida como N-Evap, esta técnica usa um coletor para direcionar múltiplos jatos finos de gás nitrogênio sobre a superfície de amostras em frascos ou microplacas. Frequentemente inclui aquecimento suave de um bloco ou banho-maria por baixo.
Isso é altamente eficaz para concentrar múltiplas amostras de pequeno volume simultaneamente e é comum na preparação de amostras para química analítica.
Evaporação Rotativa ("Rotovap")
O evaporador rotativo é o "cavalo de batalha" do laboratório de química sintética. Ele combina todos os princípios para uma remoção de solvente eficiente e suave.
- Pressão Reduzida: Uma bomba de vácuo diminui o ponto de ebulição.
- Área de Superfície Aumentada: O balão é continuamente girado, revestindo as paredes internas com uma fina película da amostra.
- Aquecimento Suave: O balão giratório fica em um banho de água para aquecimento estável e controlado.
Este método é ideal para compostos termicamente sensíveis e para remover solvente de volumes que variam tipicamente de 25 mL a vários litros.
Evaporação Centrífuga ("SpeedVac")
Um evaporador centrífugo (frequentemente chamado de SpeedVac) coloca as amostras sob vácuo profundo enquanto as gira em uma centrífuga. A força centrífuga evita a ebulição violenta, e calor suave é aplicado via radiação infravermelha.
Este é o padrão ouro para concentrar com segurança muitas amostras pequenas, preciosas ou sensíveis, como DNA, RNA ou peptídeos, sem qualquer risco de contaminação cruzada ou perda.
Entendendo as Compensações e Riscos
A escolha de um método requer equilibrar a velocidade com problemas potenciais. Estar ciente dessas compensações é fundamental para o sucesso.
Degradação da Amostra
O risco principal é a degradação térmica. Muitos compostos orgânicos e quase todas as moléculas biológicas podem ser destruídos por calor excessivo. É por isso que métodos que usam pressão reduzida, como a evaporação rotativa, são tão essenciais.
Ebulição Violenta e Perda de Amostra
Quando um líquido é aquecido sob vácuo sem agitação, ele pode superaquecer e depois ferver violentamente em uma única erupção grande. Esse fenômeno, chamado de ebulição violenta (bumping), pode fazer com que você perca uma porção significativa de sua amostra para o sistema de vácuo. A rotação (em um rotovap) ou a força centrífuga (em um SpeedVac) são usadas especificamente para evitar isso.
Remoção Incompleta do Solvente
Solventes de alto ponto de ebulição, como DMSO ou DMF, podem ser difíceis de remover completamente. Mesmo sob vácuo forte, vestígios podem permanecer, contaminando seu produto final. Isso pode ser resolvido adicionando um solvente mais volátil (como tolueno) e reevaporando, um processo conhecido como secagem azeotrópica.
Fazendo a Escolha Certa para Sua Amostra
Sua decisão deve ser guiada pelas características da sua amostra e pelo seu objetivo final.
- Se sua amostra for termicamente estável e o solvente for volátil: Evaporação simples em capela de exaustão ou sopro de nitrogênio pode ser suficiente e rápido.
- Se sua amostra for termicamente sensível ou em volume superior a 20 mL: Um evaporador rotativo é a escolha padrão e mais confiável.
- Se você tiver muitas amostras biológicas pequenas e altamente sensíveis: Um evaporador centrífugo oferece o mais alto nível de proteção e eficiência.
- Se seu objetivo é isolar um produto com pureza máxima: Sempre escolha um método com vácuo para usar a temperatura mais baixa possível, minimizando a formação de subprodutos térmicos.
Ao combinar a técnica com as necessidades da sua amostra, você garante a remoção eficiente do solvente, maximizando a integridade e o rendimento do seu produto final.
Tabela Resumo:
| Método | Melhor Para | Princípio(s) Chave |
|---|---|---|
| Evaporação Simples | Pequenos volumes de solventes não tóxicos e voláteis | Área de Superfície, Fluxo de Gás |
| Aquecimento em Placa de Aquecimento | Evaporação rápida de amostras termicamente estáveis | Temperatura |
| Sopro de Nitrogênio (N-Evap) | Concentração de múltiplas amostras de pequeno volume | Fluxo de Gás, Temperatura |
| Evaporação Rotativa (Rotovap) | Compostos termicamente sensíveis; volumes de 25mL a litros | Pressão, Área de Superfície, Temperatura |
| Evaporação Centrífuga (SpeedVac) | Amostras biológicas pequenas, preciosas ou sensíveis | Pressão, Força Centrífuga |
Precisa Otimizar Seu Processo de Evaporação de Solvente?
A escolha do equipamento certo é fundamental para proteger suas amostras sensíveis e maximizar o rendimento. A KINTEK é especializada em fornecer equipamentos de laboratório e consumíveis confiáveis, adaptados às necessidades exclusivas do seu laboratório.
Se você precisa de um evaporador rotativo suave para seus fluxos de trabalho de química sintética ou de um evaporador centrífugo de alto rendimento para amostras biológicas preciosas, nós temos a solução.
Deixe nossos especialistas ajudá-lo a aumentar a eficiência do seu laboratório e a integridade da amostra.
Entre em contato com a KINTEK hoje mesmo para encontrar o sistema de evaporação perfeito para sua aplicação!
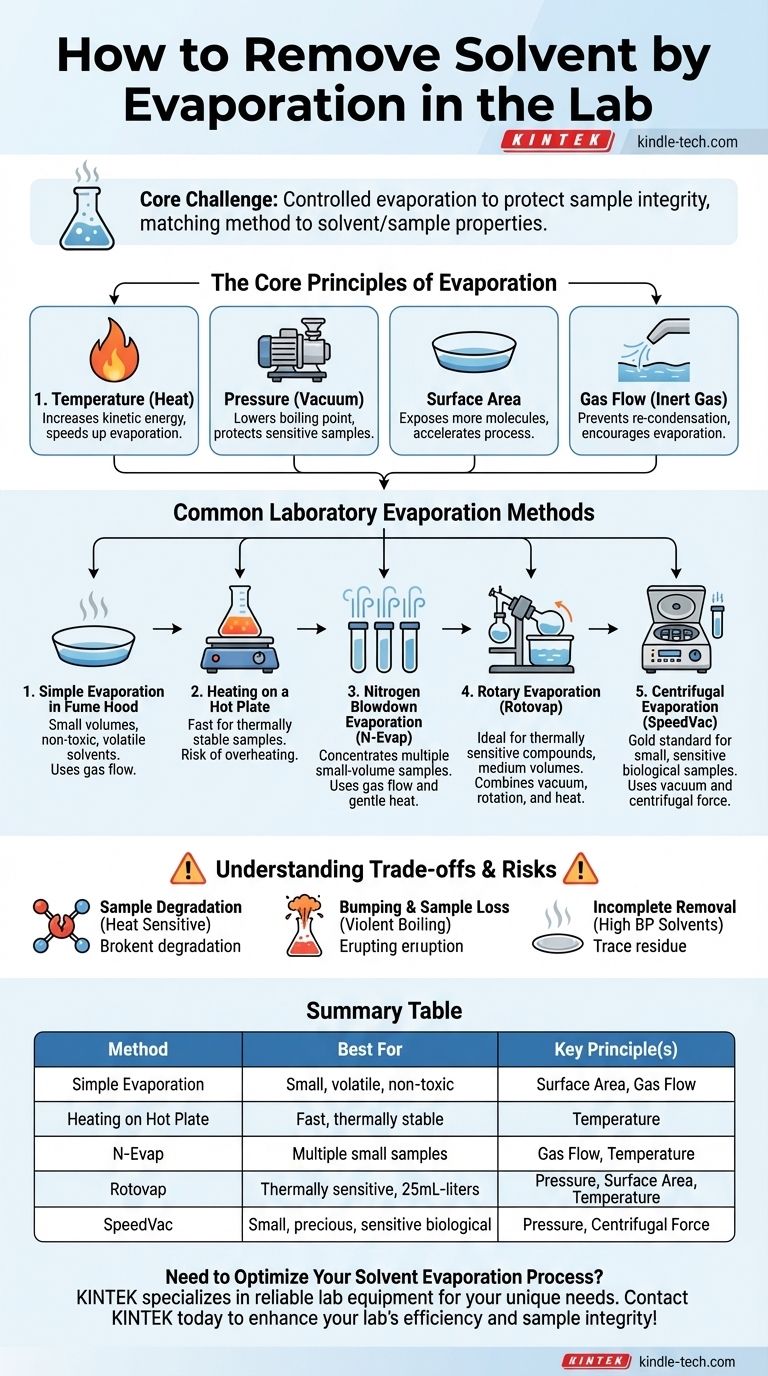
Guia Visual
Produtos relacionados
- Forno de Tubo de Deposição Química de Vapor Assistida por Plasma (PECVD) Rotativo Inclinado
- Equipamento de Deposição Química em Fase de Vapor Aprimorada por Plasma Rotativo Inclinado PECVD Forno Tubular
- Forno de Tubo Rotativo de Inclinação a Vácuo de Laboratório Forno de Tubo Rotativo
- Forno de Tubo Rotativo Split com Múltiplas Zonas de Aquecimento Forno de Tubo Rotativo
- Forno de Tubo Rotativo de Trabalho Contínuo com Vedação a Vácuo Forno de Tubo Giratório
As pessoas também perguntam
- Qual é o processo de PECVD na fabricação de semicondutores? Possibilitando a deposição de filmes finos a baixa temperatura
- Quais são as vantagens da deposição química de vapor assistida por plasma? Permite a deposição de filmes de alta qualidade a baixas temperaturas
- Para que serve a deposição química de vapor assistida por plasma (PECVD)? Habilitar filmes finos de baixa temperatura para eletrônicos e solar
- Quais são os benefícios da deposição química de vapor assistida por plasma? Obtenha Deposição de Filmes de Alta Qualidade e Baixa Temperatura
- Quais são as principais vantagens do PE-CVD na encapsulação de OLED? Proteja Camadas Sensíveis com Deposição de Filmes a Baixa Temperatura



















