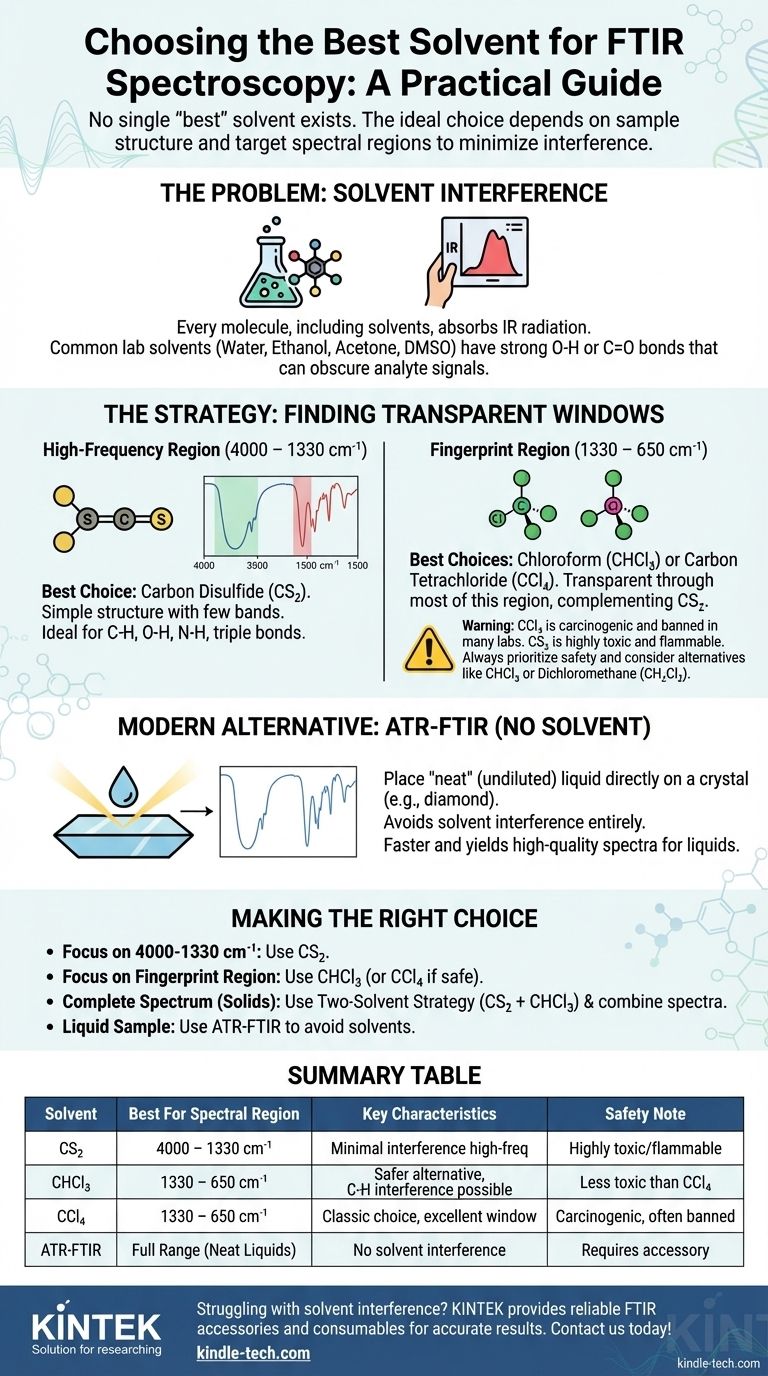
Em resumo, não existe um único solvente "melhor" para a espectroscopia FTIR. A escolha ideal depende inteiramente da estrutura química da sua amostra e das regiões espectrais específicas que você precisa analisar. A abordagem mais comum e eficaz envolve o uso de solventes como dissulfeto de carbono (CS₂) e tetracloreto de carbono (CCl₄) ou clorofórmio (CHCl₃), porque suas próprias bandas de absorção são simples e previsíveis, deixando grandes "janelas" de transparência para visualizar o composto de interesse.
O principal desafio na seleção de solventes em FTIR é que todo solvente absorve radiação infravermelha em algum grau. A estratégia, portanto, não é encontrar um solvente perfeitamente "invisível", mas sim escolher aquele cujas bandas de absorção não se sobreponham às bandas vibracionais importantes do seu analito.

O Problema: Interferência do Solvente
Toda molécula, incluindo uma molécula de solvente, é composta por ligações químicas que vibram quando expostas à radiação infravermelha. Essas vibrações causam bandas de absorção em um espectro de IR.
O Ideal vs. A Realidade
Um solvente ideal seria "transparente ao IR", o que significa que ele não teria vibrações que absorvem radiação na faixa do infravermelho médio (4000-400 cm⁻¹). Nenhum solvente assim existe.
O objetivo é selecionar um solvente que interfira o mínimo possível. Isso geralmente significa uma molécula pequena e simples com poucas ou nenhuma ligação correspondente a grupos funcionais comuns, como O-H, N-H ou C=O.
Por Que Solventes Comuns de Laboratório Falham
Solventes como água, etanol, acetona e DMSO são geralmente más escolhas para FTIR de transmissão. Eles contêm ligações O-H ou C=O, que absorvem muito fortemente e criam picos largos e intensos que podem facilmente obscurecer todo o espectro da amostra dissolvida.
Um Guia Prático para Solventes Comuns de FTIR
A melhor prática geralmente envolve o uso de um par de solventes para montar um espectro completo. Um solvente é usado para a região de alta frequência e outro para a região de "impressão digital" de baixa frequência.
Para a Região de Alta Frequência (4000 – 1330 cm⁻¹)
O Dissulfeto de Carbono (CS₂) é a principal escolha para esta região.
Sua estrutura simples e linear (S=C=S) significa que ele tem apenas algumas bandas de absorção. É amplamente transparente onde aparecem os estiramentos de C-H, O-H, N-H e ligações triplas, tornando-o ideal para analisar esses grupos funcionais críticos. Sua principal interferência é uma banda forte em torno de 1535-1485 cm⁻¹.
Para a Região de Impressão Digital (1330 – 400 cm⁻¹)
O Tetracloreto de Carbono (CCl₄) é a escolha clássica para esta região.
É uma molécula simples e simétrica que é transparente em grande parte da faixa do infravermelho médio, mas possui absorções muito fortes abaixo de ~800 cm⁻¹. Isso o torna o complemento perfeito para o CS₂, pois sua "janela" de transparência cobre a região onde o CS₂ absorve.
Alternativas Modernas e Mais Seguras
O Clorofórmio (CHCl₃) e o Diclorometano (CH₂Cl₂) são frequentemente usados como alternativas mais práticas e menos tóxicas ao CCl₄.
Eles são solventes de uso geral melhores, mas possuem mais ligações C-H, o que significa que têm mais picos de interferência do que o CCl₄. No entanto, eles ainda oferecem janelas grandes e úteis e são um bom compromisso entre clareza espectral e utilidade do solvente. O clorofórmio, por exemplo, é uma boa escolha para a região de impressão digital, mas possui bandas C-H que interferirão em torno de 3000 cm⁻¹ e 1200 cm⁻¹.
Entendendo as Compensações
A escolha de um solvente é um ato de equilíbrio entre clareza espectral, solubilidade da sua amostra e segurança.
A Estratégia de Dois Solventes
O método mais rigoroso para obter um espectro completo de um composto solúvel é realizar dois experimentos separados:
- Dissolva a amostra em dissulfeto de carbono (CS₂) para obter uma visão clara da região de 4000 – 1330 cm⁻¹.
- Dissolva uma segunda amostra em clorofórmio (CHCl₃) ou CCl₄ para obter uma visão clara da região de 1330 – 650 cm⁻¹.
Em seguida, você pode combinar digitalmente as porções úteis de ambos os espectros para criar um espectro completo e livre de interferências.
A Questão Crítica da Toxicidade
Muitos dos "melhores" solventes para FTIR são perigosos. O tetracloreto de carbono é um carcinógeno conhecido e é banido na maioria dos laboratórios modernos. O dissulfeto de carbono é altamente tóxico e extremamente inflamável.
Sempre consulte uma Ficha de Dados de Segurança (SDS) e use equipamento de proteção individual (EPI) apropriado, incluindo trabalhar em uma capela de exaustão, ao manusear esses produtos químicos. A segurança geralmente dita o uso de um solvente ligeiramente menos "perfeito", mas mais seguro, como clorofórmio ou diclorometano.
A Alternativa Moderna: Nenhum Solvente
Para muitas amostras líquidas, o melhor solvente é nenhum solvente. A Reflectância Total Atenuada (ATR) é uma técnica de amostragem moderna que revolucionou a análise FTIR de rotina.
ATR-FTIR permite que você coloque uma única gota de um líquido "puro" (não diluído) diretamente em uma superfície de cristal (geralmente diamante). O feixe de IR interage com a amostra na interface, produzindo um espectro de alta qualidade sem qualquer interferência do solvente. Se sua amostra for líquida e você tiver um acessório ATR, é quase sempre mais rápido, mais fácil e produz um espectro mais limpo do que o método de transmissão tradicional.
Fazendo a Escolha Certa para Sua Análise
- Se seu foco principal for a região de C-H, N-H, O-H ou alcino (4000-1330 cm⁻¹): Sua melhor escolha é o dissulfeto de carbono (CS₂).
- Se seu foco principal for a região de impressão digital (1330-650 cm⁻¹): Sua melhor escolha é o clorofórmio (CHCl₃) ou, se os protocolos de segurança permitirem, o tetracloreto de carbono (CCl₄).
- Se você precisar de um espectro completo de qualidade de publicação de um sólido: Use a estratégia de dois solventes, combinando um espectro de CS₂ com um de CHCl₃.
- Se sua amostra for líquida e você quiser evitar totalmente a interferência do solvente: Use um acessório ATR-FTIR para analisar o líquido puro diretamente.
Ao entender que o objetivo é encontrar janelas espectrais, você pode selecionar com confiança um solvente que revele a estrutura da sua amostra em vez de obscurecê-la.
Tabela de Resumo:
| Solvente | Melhor Para Região Espectral | Características Principais |
|---|---|---|
| Dissulfeto de Carbono (CS₂) | 4000 – 1330 cm⁻¹ (C-H, O-H, N-H) | Interferência mínima na região de alta frequência; altamente tóxico/inflamável |
| Clorofórmio (CHCl₃) | 1330 – 650 cm⁻¹ (Região de impressão digital) | Alternativa mais segura ao CCl₄; bom para análise de impressão digital |
| Tetracloreto de Carbono (CCl₄) | 1330 – 650 cm⁻¹ (Região de impressão digital) | Escolha clássica, mas cancerígena; amplamente banida |
| ATR-FTIR (Sem Solvente) | Faixa completa (Líquidos puros) | Técnica moderna; evita completamente a interferência do solvente |
Com dificuldades com a interferência do solvente em sua análise FTIR? A KINTEK é especializada em equipamentos e consumíveis de laboratório, fornecendo acessórios e solventes FTIR confiáveis adaptados às necessidades do seu laboratório. Se você está otimizando a clareza espectral ou garantindo a conformidade com as normas de segurança, nossa experiência ajuda você a obter resultados precisos e livres de interferência. Entre em contato conosco hoje para encontrar a solução perfeita para seus desafios de FTIR!
Guia Visual
Produtos relacionados
- Banho de Água de Célula Eletroquímica Eletrolítica Multifuncional Camada Única Dupla Camada
- Crisol de Evaporação para Matéria Orgânica
- Eletrodo de Referência Calomelano Cloreto de Prata Sulfato de Mercúrio para Uso Laboratorial
- Circulador de Arrefecimento de 10L Banho de Água de Arrefecimento Banho de Reação de Temperatura Constante de Baixa Temperatura
- Circulador de Refrigeração e Aquecimento de 5L para Banho de Água de Refrigeração para Reação de Temperatura Constante Alta e Baixa
As pessoas também perguntam
- Quais são as diretrizes para a esterilização em alta temperatura da célula eletrolítica multifuncional? Evite danos permanentes à sua tampa de PTFE
- Quando é necessário reparo profissional para uma célula eletrolítica de banho-maria de dupla camada? Proteja a Precisão e a Segurança do Seu Laboratório
- Como prevenir vazamentos de água e gás em uma célula eletrolítica de banho-maria de dupla camada? Um guia para manutenção proativa
- O que envolve a manutenção de rotina de uma célula eletrolítica de banho-maria de dupla camada? Um guia para garantir precisão e longevidade
- Quais são os procedimentos após o uso de uma célula eletrolítica de banho-maria de dupla camada? Garanta a Longevidade do Equipamento e a Precisão dos Dados



















